��Ŀ����
5��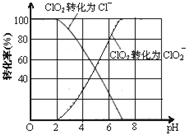 ��֪����ClO2����ֻ�ܱ�����Ũ�Ƚϵ�״̬���Է�ֹ��ը�Էֽ⣬�����ֺϳ����ã���ClO2���������Ժͼ�����Һ�в����ȶ����ڣ�
��֪����ClO2����ֻ�ܱ�����Ũ�Ƚϵ�״̬���Է�ֹ��ը�Էֽ⣬�����ֺϳ����ã���ClO2���������Ժͼ�����Һ�в����ȶ����ڣ���1��ClO2��S2-��ԭΪClO2-��Cl-ת������pH��ϵ��ͼ��pH��2ʱClO2��S2-��Ӧ�����ӷ���ʽ��2ClO2+5S2-+8H+=2Cl-+5S��+4H2O
��2��ClO2����ˮ��Fe2+��Mn2+��S2-��CN-�������Ե�ȥ��Ч����ij������ˮ�к�CN-amg/L������ClO2��CN-�������������������������壬�����ӷ�Ӧ����ʽΪ2ClO2+2CN-=N2��+2CO2��+2Cl-����100m3������ˮ��������ҪClO2$\frac{50a}{13}$ mol��
���� ��1������ͼ���֪��pH��2ʱClO2����ԭΪCl-������������ԭ��Ӧ�Ĺ��ɽ�ϵ����غ�����д����ʽ��
��2��ClO2��CN-������ֻ�����������壬Ӧ���ɵ����������̼��ͬʱ���������ӣ����ݷ���ʽ������ҪClO2�����ʵ�����
��� �⣺��1������ͼ���֪��pH��2ʱClO2����ԭΪCl-�����Ը÷�Ӧ�����ӷ���ʽ��2ClO2+5S2-+8H+=2Cl-+5S��+4H2O��
�ʴ�Ϊ��2ClO2+5S2-+8H+=2Cl-+5S��+4H2O��
��2��ClO2��CN-������ֻ�����������壬Ӧ���ɵ����������̼��ͬʱ���������ӣ���Ӧ���ӷ���ʽΪ��2ClO2+2CN-=N2��+2CO2��+2Cl-��
100m3��ˮ��CN-����=100m3��ag/m3=100ag��CN-�����ʵ���Ϊ$\frac{100ag}{26g/mol}$=$\frac{50a}{13}$mol���ɷ���ʽ��֪��������ҪClO2�����ʵ���=$\frac{50a}{13}$mol��
�ʴ�Ϊ��2ClO2+2CN-=N2��+2CO2��+2Cl-��$\frac{50a}{13}$mol��
���� ���⿼��ѧ���Ķ���Ŀ��ȡ��Ϣ����������Ũ�ȸ�������⡢��������ԭ��Ӧ���֪ʶ�����á��й�ʵ������ͼ�ʵ��������������Լ������龳���ۺ�����֪ʶ����������������Ŀ��һ�����Ѷȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | Fe+2FeCl3�T3FeCl2 | B�� | CH4+2O2=CO2+2H2O | ||
| C�� | H2+Cl2=2HCl | D�� | H2SO4+2NaOH�TNa2SO4+2H2O |
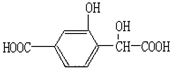 ij�л���Ľṹ��ʽ��ͼ��ʾ��1mol�ĸ��л���ֱ��������Na��NaOH��NaHCO3��Ӧʱ�������������ʵ����ʵ���֮���ǣ�������
ij�л���Ľṹ��ʽ��ͼ��ʾ��1mol�ĸ��л���ֱ��������Na��NaOH��NaHCO3��Ӧʱ�������������ʵ����ʵ���֮���ǣ�������| A�� | 1��1��1 | B�� | 1��1��2 | C�� | 4��3��2 | D�� | 2��3��2 |
| A�� | �ձ�����Ͳ������ƿ������Һ����ʱ������ֱ���ܽ����� | |
| B�� | ���ȵ��Թܡ��ձ�����������������ɷ���ʵ��̨����ȴ | |
| C�� | ����ƿ���ζ��ܡ�����©��ʹ��ǰ��Ҫ��© | |
| D�� | ��������ƽ�������������ʳ��ʱ�����������ϵ�ȴ�İ�ֽ���� |
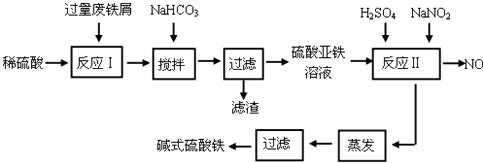
��֪������������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe��OH��3 | Fe��OH��2 | Al��OH��3 |
| ��ʼ���� | 2.3 | 7.5 | 3.4 |
| ��ȫ���� | 3.2 | 9.7 | 4.4 |
��1����������NaHCO3��Ŀ���ǵ���pH��4.4��7.5��Χ�ڣ�ʹ��Һ�е�Al3+������д���ӷ��ţ���
��2����Ӧ���м���NaNO2��Ŀ��������Fe2+��������Ӧ�����ӷ���ʽΪ2H++Fe2++NO2-=Fe3++NO��+H2O��
��3����ʵ�������У���Ӧ��ͬʱͨ��O2�Լ���NaNO2�������������뷴Ӧ��O2��11.2L����״���������൱�ڽ�ԼNaNO2�����ʵ���Ϊ2mol��
��4����ʽ����������ˮ�������Fe��OH��2+���ӣ�Fe��OH��2+�ɲ���ˮ������Fe2��OH��42+�ۺ����ӣ���ˮ�ⷴӦ�����ӷ���ʽΪ2Fe��OH��2++2H2O=Fe2��OH��42++2H+��
| A�� | CH3CH2CH3��C3H8 | B�� | -NO2��NO2 | C�� | -OH��OH- | D�� | C3H6��CH3CH=CH2 |
| A�� | ������������ | B�� | ���ۺ���ά�� | C�� | �����Ǻ��� | D�� | ���Ǻ���ѿ�� |


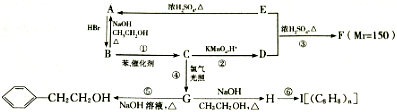
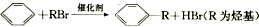 ��
�� ����������ϡ��������������
����������ϡ�������������� ��
�� ��
��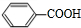 +CH3CH2OH$��_{��}^{Ũ����}$
+CH3CH2OH$��_{��}^{Ũ����}$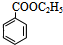 +H2O��
+H2O�� ��
��
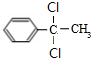 ��
��