题目内容
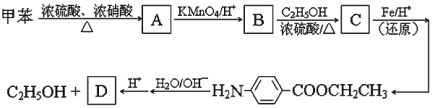
【题目】反-2-己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一。根据该合成路线回答下列问题:

已知:
![]() RCHO+R'OH+R"OH
RCHO+R'OH+R"OH
(1)A的名称是__________;B分子中共面原子数目最多为__________;C分子中与环相连的三个基团中,不同化学环境的氢原子共有__________种。
(2)D中含氧官能团的名称是__________,写出检验该官能团的化学反应方程式:__________。
(3)E为有机物,能发生的反应有__________。
a.聚合反应b.加成反应c.消去反应d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:________。
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充完整。

(6)问题(5)的合成路线中第一步反应的目的是__________。
【答案】(1)正丁醛或丁醛 9 8
(2)醛基
![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
 +2Ag↓+3NH3+H2O或
+2Ag↓+3NH3+H2O或![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
 +Cu2O↓+3H2O;
+Cu2O↓+3H2O;
(3)cd;
(4)CH2=CHCH2OCH3、![]() 、
、![]() 、
、![]() ;
;
(5)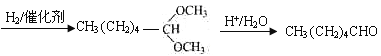 ;
;
(6)保护醛基(或其他合理答案)
【解析】试题分析:(1)根据流程图,A为CH3CH2CH2CHO,是丁醛;B为CH2=CHOC2H5,分子中共面原子数目最多为9个(如图: ),C分子中与环相连的三个基团中,8个碳原子上的氢原子化学环境都不相同,共有8种,故答案为:丁醛;9;8;
),C分子中与环相连的三个基团中,8个碳原子上的氢原子化学环境都不相同,共有8种,故答案为:丁醛;9;8;
(2)D为![]() ,其中含氧官能团是醛基,检验醛基可以用银氨溶液或新制氢氧化铜悬浊液,故答案为:醛基;
,其中含氧官能团是醛基,检验醛基可以用银氨溶液或新制氢氧化铜悬浊液,故答案为:醛基;![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
 +2Ag↓+3NH3+H2O或
+2Ag↓+3NH3+H2O或![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
 +Cu2O↓+3H2O;
+Cu2O↓+3H2O;
(3)根据流程图,结合信息,C在酸性条件下反应生成![]() 、CH3CH2CH2CHO和CH3CH2OH以及水,因此E为CH3CH2OH,属于醇,能发生的反应有消去反应和取代反应,故选cd;
、CH3CH2CH2CHO和CH3CH2OH以及水,因此E为CH3CH2OH,属于醇,能发生的反应有消去反应和取代反应,故选cd;
(4)B的同分异构体F与B有完全相同的官能团, F可能的结构有:CH2=CHCH2OCH3![]() 、
、![]() 、
、![]() ,故答案为:CH2=CHCH2OCH3
,故答案为:CH2=CHCH2OCH3![]() 、
、![]() 、
、![]() ;
;
(5)D为![]() ,己醛的结构简式为CH3CH2CH2CH2CH2CHO,根据信息和己醛的结构,
,己醛的结构简式为CH3CH2CH2CH2CH2CHO,根据信息和己醛的结构, 首先需要将碳碳双键转化为单键,然后在酸性条件下反应即可,故答案为:
首先需要将碳碳双键转化为单键,然后在酸性条件下反应即可,故答案为: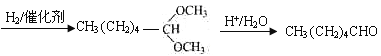 ;
;
(6)醛基也能够与氢气加成,(5)中合成路线中第一步反应的目的是保护醛基,故答案为:保护醛基。

【题目】已知:实验室常用无水乙醇(CH3CH2OH)制备乙烯,制备原理为:
CH3CH2OH![]() CH2=CH2↑+H2O。
CH2=CH2↑+H2O。
无水乙醇性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 挥发性 | 化学性质 |
无水乙醇 | —114.1 | 78.3 | 能与水以任意比互溶 | 易挥发 | 能使酸性高锰酸钾溶液褪色 |
甲、乙同学用下列实验装置制备乙烯并验证其性质。(气密性已检验,部分夹持装置略)。

实验操作和现象:
操 作 | 现 象 |
点燃酒精灯,加热至170℃ | I:A中烧瓶内液体渐渐变黑 II:B内气泡连续冒出,溶液逐渐褪色 |
…… | |
实验完毕,清洗烧瓶 | III:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)写出乙烯的1个用途: ,对应方程式为(注明反应类型) 。
(2)A中烧瓶内溶液“渐渐变黑”,说明浓硫酸具有 性。
(3)分析使B中溶液褪色的物质,甲认为是C2H4使B中溶液褪色,该反应的化学方程式为(注明反应类型) 。
(4)乙根据反应原理及现象I和III综合分析,认为产物中除乙烯外还混有乙醇、H2O、CO2和一种 “有刺激性气味”的气体X。你认为这种“有刺激性气味”气体X是 (填化学式)。
为验证气体X的存在,并证实是C2H4使B中溶液褪色,乙设计如下装置,与A连接:
设 计 | 现 象 |
与A连接的装置如下:
| C中溶液褪色,加热后又恢复红色; F中溶液褪色 |
请回答下列问题:
D中盛放的试剂是 (填化学式),不能盛放酸性KMnO4溶液的原因是(用离子方程式解释): 。