��Ŀ����
����Ŀ��ʵ�����ù���NaOH����0.5 mol/L��NaOH��Һ500 mL�����ձ���100 ml��Ͳ������ƿ��ҩ�עݲ�������������ƽ����ƿ
��1������ʱ������ʹ�õ�������_____________(�����)����ȱ�ٵ�������__________________��
��2�������Ƶ�ת�ƹ�����ijѧ��������ͼ��������ָ�����еĴ���______________��____________��
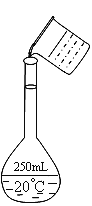
��3������ʱ��һ��ɷ�Ϊ���¼�������ٳ����ڼ�����ܽ��ҡ�Ȣ�ת�Ƣ�ϴ�Ӣ߶��ݢ���ȴ������ȷ�IJ���˳��Ϊ_________________��
��4�����в�����ʹ���Ƶ���ҺŨ��ƫ�͵���___________(����ĸ)
A.û�н�ϴ��Һת�Ƶ�����ƿ B.ת�ƹ�������������Һ����
C.����ƿϴ����δ���� D.����ʱ���ӿ̶���
E.����NaOH�������Na2O����
��5��������ƿʹ�÷����У����в�������ȷ����(�����) ___________
A.ʹ������ƿǰ������Ƿ�©ˮ
B.����ƿ������ˮϴ�������ü�Һ��ϴ
C.���������ƹ���ֱ�ӷ�����ƽ���̵���ֽ�ϣ�ȷ�����������ձ����ܽ������ע������ƿ��
D.���ݺ�����ƿ������ʳָ��סƿ��������һֻ�ֵ���ָ��סƿ�ף�������ƿ��תҡ��
���𰸡� �٢ۢܢݢ� ��ͷ�ι� δ�ò��������� ʹ����250mL������ƿ����ûʹ��500mL������ƿ�� �ڢ٢ۢ�ݢޢߢ����ڢ٢ۢ�ݢޢܢߢ� AB BC
����������1�����������м��㡢�������ܽ⡢��Һ��ϴ����Һ�����ݡ�ҡ�ȵȲ�����һ����������ƽ��������ҩ��ȡ��ҩƷ�����ձ����ܽ⣬���ò��������裬�����ܽ⣬��ȴ��ת�Ƶ�100mL����ƿ�У����ò�����������ϴ���ձ���������2-3�Σ�����ϴ��Һ��������ƿ�У���ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�����ݵߵ�ҡ�ȣ�������Ҫ�������У���ƽ���ձ�����������500mL����ƿ����ͷ�ιܡ�ҩ�ס�����ʱ������ʹ�õ��������٢ۢܢݢ�(�����)����ȱ�ٵ������ǽ�ͷ�ι�����2������NaOH��Һ500mL��Ҫ��500mL����ƿ��������ƿ����Һ��Ҫ�ò�������������3������ʱ��һ��ɷ�Ϊ���¼�������ٳ����ڼ�����ܽ��ҡ�Ȣ�ת�Ƣ�ϴ�Ӣ߶��ݢ���ȴ������ȷ�IJ���˳��Ϊ�ڢ٢ۢ�ݢޢߢ����ڢ٢ۢ�ݢޢܢߢ� ����4��A��û�н�ϴ��Һת�Ƶ�����ƿ������ת�Ƶ�����ƿ�����ʵ����ʵ���ƫС������Ũ�ȹ�ʽ��֪��������ҺŨ��ƫ�ͣ���A��ȷ��B��ת�ƹ�������������Һ����������ת�Ƶ�����ƿ�����ʵ����ʵ���ƫС������Ũ�ȹ�ʽ��֪��������ҺŨ��ƫ�ͣ���B��ȷ��C������ʱ����������ƿ�м���ˮ����������ƿϴ����δ�����ʵ����Ӱ�죬��C���� D������ʱ���ӿ̶��ߣ������¼��������ˮƫ�٣���Һ�����ƫС������Ũ�ȹ�ʽ��֪��������ҺŨ��ƫ�ߣ���D����E������NaOH�к�������Na2O���ʣ�Na2O��ˮ��Ӧ����NaOH��ʹNaOH�����ʵ���ƫ�࣬����Ũ�ȹ�ʽ��֪��������ҺŨ��ƫ�ߣ���E����ѡAB����5��A����������跴���ߵ�ҡ�ȣ���ʹ������ƿǰ������Ƿ�©ˮ����A��ȷ��B������ƿ������ˮϴ�������ü�Һ��ϴ����ʹ������ҺŨ��ƫ�ߣ���B����C�����������ܽ�ʱ�ų��������ȣ���ȴ����������Һ�����ƫС��������ƿ���Ȳ��������ܵ������ѣ�����������ƿ���ܽ��������ƣ���C����D��ҡ��ʱʳָ��סƿ��������һֻ�ֵ���ָ��סƿ�ף�������ƿ��ת��������ҡ�ȣ���D��ȷ����ѡBC��


