题目内容
8.按要求填空:(1)写出下列反应的化学方程式:
①实验室制取氨气2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
②浓硝酸的见光分解4HNO3 $\frac{\underline{\;\;△\;\;}}{\;}$O2+4NO2↑+2H2O
③二氧化氮和水反应3NO2+H2O═NO+2HNO3
(2)(10分)A、B、C、D为中学常见物质且均含有同一种元素,相互转化关系如图(反应条件及其他物质已经略去):A$\stackrel{+O_{2}}{→}$B$\stackrel{+O_{2}}{→}$C$\stackrel{+H_{2}O}{→}$D
①若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,则D为(填写化学式):H2SO4.写出B→C的化学方程式:2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3.
②若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红.则D的化学式为HNO3.写出A→B的化学方程式:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O.
③若A为单质,组成元素的原子所含质子的数目小于18,D为强碱,写出C→D的化学方程式:2Na2O2+2H2O═4NaOH+O2↑.
分析 (1)①实验室利用氯化铵与氢氧化钙再加热条件下制备氨气,反应生成氯化钙、氨气与水;
②浓硝酸见光分解生成二氧化氮与氧气、水;
③二氧化氮和水反应是硝酸与NO;
(2)①若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,它们的水溶液均呈酸性,则A为H2S,B为SO2,C为SO3,D为H2SO4;
②若A的水溶液能使湿润的红色石蕊试纸变蓝,则A为NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,D呈酸性,则B为NO,C为NO2,D为HNO3;
③若A为单质,组成元素的原子所含质子的数目小于18,D为强碱,则A为Na,B为Na2O,C为Na2O2,D为NaOH.
解答 解:(1)①实验室利用氯化铵与氢氧化钙再加热条件下制备氨气,反应生成氯化钙、氨气与水,反应方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②浓硝酸见光分解生成二氧化氮与氧气、水,反应方程式为:4HNO3 $\frac{\underline{\;\;△\;\;}}{\;}$O2+4NO2↑+2H2O,
故答案为:4HNO3 $\frac{\underline{\;\;△\;\;}}{\;}$O2+4NO2↑+2H2O;
③二氧化氮和水反应是硝酸与NO,反应方程式为:3NO2+H2O═NO+2HNO3,
故答案为:3NO2+H2O═NO+2HNO3;
(2)①若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,它们的水溶液均呈酸性,则A为H2S,B为SO2,C为SO3,D为H2SO4,B→C的化学方程式:2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3,
故答案为:H2SO4;2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3;
②若A的水溶液能使湿润的红色石蕊试纸变蓝,则A为NH3,D的稀溶液能使湿润的蓝色石蕊试纸变红,D呈酸性,则B为NO,C为NO2,D为HNO3,A→B的化学方程式:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O,
故答案为:HNO3;4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O;
③若A为单质,组成元素的原子所含质子的数目小于18,D为强碱,则A为Na,B为Na2O,C为Na2O2,D为NaOH,C→D的化学方程式:2Na2O2+2H2O═4NaOH+O2↑,
故答案为:2Na2O2+2H2O═4NaOH+O2↑.
点评 本题考查无机物推断,涉及S、N、Na元素及其化合物的性质与转化,需要学生熟练掌握元素化合物性质,难度不大.

| A. | SO2、H2S、O2 | B. | CO、H2、Cl2 | C. | NO、H2、O2 | D. | HCl、CO、NH3 |
| A. | Fe3O4 | B. | HF | C. | FeCl2 | D. | CuCl2 |
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ①⑤ |
| A. | C | B. | Si | C. | S | D. | C1 |
| A. | 生石灰加水制熟石灰 | B. | 化石燃料的燃烧 | ||
| C. | 氢氧化钠溶液中滴加稀盐酸 | D. | 二氧化碳与高温的炭 |
 有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4mol淡黄色粉末时,产生气体0.3mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如图所示.
有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4mol淡黄色粉末时,产生气体0.3mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如图所示.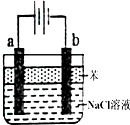 (1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
 (或写成
(或写成 R代表取代基或氢)
R代表取代基或氢) .
. .
.