题目内容
已知电离平衡常数:H2CO3>HClO>HCO,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是
| A.向FeI2溶液中滴加少量氯水,反应的离子方程式为2Fe2++Cl2=3Fe3++2Cl- |
| B.向溴水中加入足量氯化亚铁溶液能使溴水变成无色 |
C.向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+ |
| D.能使pH试纸显深红色的溶液,Fe3+、Cl-、Ba2+、Br-能大量共存 |
D
解析

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A.大理石与盐酸反应:CO32-+ 2H+=H2O+CO2↑ |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-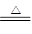 NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
在加入铝粉能放出氢气的溶液中,下列各组离子可能大量共存的是
| A.NH4+、NO3-、CO32-、Na+ | B.Na+、Ba2+、HCO3-、AlO2- |
| C.NO3-、K+、AlO2-、OH- | D.NO3-、Mg 2+、K+、CH3COO- |
在加入铝粉能放出H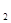 的溶液中,下列各组离子一定不能大量共存的是( )
的溶液中,下列各组离子一定不能大量共存的是( )
A.Na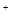 、Fe 、Fe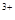 、SO 、SO 、Cl 、Cl |
B.Ba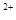 、Mg 、Mg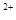 、HCO 、HCO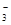 、NO 、NO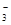 |
C.Na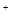 、K 、K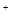 、NO 、NO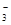 、CO 、CO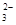 |
D.K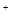 、NO 、NO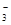 、AlO 、AlO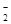 、OH 、OH |
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能溶解Al2O3的溶液:Na+、K+、 、 、 |
| B.0.1 mol·L-1Ca(ClO)2溶液:K+、Na+、I-、Cl- |
C.能使甲基橙显红色的溶液:K+、Fe2+、Cl-、 |
D.加入KSCN显红色的溶液:Na+、Mg2+、Cl-、 |
下列离子方程式或化学方程式与所述事实相符且正确的是
A.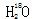 中投入Na2O2固体: 中投入Na2O2固体: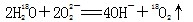 |
| B.向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:H++OH- =H2O |
| C.以金属银为阳极电解饱和硫酸铜溶液:Cu2++2H2O=2Cu+O2↑+4H+ |
D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使 完全沉淀:Al3++2 完全沉淀:Al3++2 +2Ba2++4OH-= +2Ba2++4OH-= +2BaSO4↓+2H2O +2BaSO4↓+2H2O |
某溶液中含有NO、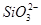 、
、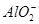 、S2-4种离子,若向其中加入过量的盐酸,微热并搅拌,再加入过量的氢氧化钠溶液,则溶液中离子数目大量减少的是
、S2-4种离子,若向其中加入过量的盐酸,微热并搅拌,再加入过量的氢氧化钠溶液,则溶液中离子数目大量减少的是
| A.只有S2- | B.S2-和NO3- |
C.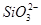 、S2-和NO3- 、S2-和NO3- | D.4种离子都减少 |
某废水中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2一、CO32-、S2一、SO32-、SO42-
现取该溶液进行有关实验,实验过程及现象如下: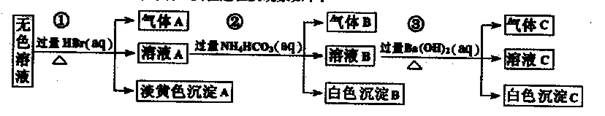
下列说法正确的是
| A.根据实验①中的现象可推出,气体A一定是纯净物,淡黄色沉淀一定是AgBr |
| B.根据实验②中的现象可推出,气体B是CO2,沉淀B是Al(OH)3,原溶液中一定含有Al3+ |
| C.根据实验③中的现象可推出,气体C是NH3,沉淀C一定有BaCO3,可能有BaSO4 |
| D.原溶液中肯定含有Na+、AlO2-、S2-,不能确定是否含有SO32-、SO42- |
 =CaCO3↓+
=CaCO3↓+