题目内容
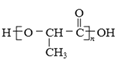
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
【答案】A
【解析】根据能量守恒,则反应物的总能量高于生成物的总能量,该反应为放热反应,锌和硫酸反应为放热反应, A正确;反应物的总能量高于生成物的总能量,反应物和生成物均有两种,无法比较1molZn和1molH2的能量大小,B错误;若将其设计为原电池,锌化合价升高,失电子,则锌作负极,C错误;若将其设计为原电池,当有32.5gZn溶解时,消耗锌的物质的量为0.5mol,根据反应方程式可知生成0.5molH2,但气体所处状态未知,不能确定气体体积,D错误;正确选项A。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
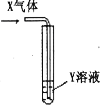
【题目】将足量X气体通入Y溶液中,实验结果与预测现象一致的组合是( )
X气体 | Y溶液 | 预测现象 |
| |
① | CO2 | Na2SiO3溶液 | 有白色沉淀产生 | |
② | SO2 | BaCl2溶液 | 有白色沉淀产生 | |
③ | Cl2 | AgNO3溶液 | 有白色沉淀产生 | |
④ | NH3 | AlCl3溶液 | 有白色沉淀产生 |
A.只有①②③B.只有①②④
C.只有①③④D.①②③④