题目内容
按照要求回答下列问题写出下列变化的化学方程式:
(1)实验室制乙烯(注明反应条件)______.
(2)乙烯→氯乙烷______.
已知:甲酸和乙酸相类似,具有下列性质:①挥发性 ②酸性 ③比碳酸的酸性强 ④还原性 ⑤能发生酯化反应.
下列各实验中,分别填出表现甲酸相应性质的编号:
(3)在碳酸钠溶液中加入甲酸有气体放出,说明甲酸具有______
(4)在甲酸钠晶体中加入浓磷酸,加热后放出能使湿润蓝色石蕊试纸变红的气体,说明甲酸具有______
(5)与乙醇、浓硫酸混和后共热,能闻到一种香味,说明甲酸具有
(6)在甲酸溶液中加入氢氧化铜,能看到溶液变蓝色,说明甲酸具有______
(7)在新制氢氧化铜中加入甲酸溶液,加热看到有红色沉淀生成,说明甲酸具有______.
(1)实验室制乙烯(注明反应条件)______.
(2)乙烯→氯乙烷______.
已知:甲酸和乙酸相类似,具有下列性质:①挥发性 ②酸性 ③比碳酸的酸性强 ④还原性 ⑤能发生酯化反应.
下列各实验中,分别填出表现甲酸相应性质的编号:
(3)在碳酸钠溶液中加入甲酸有气体放出,说明甲酸具有______
(4)在甲酸钠晶体中加入浓磷酸,加热后放出能使湿润蓝色石蕊试纸变红的气体,说明甲酸具有______
(5)与乙醇、浓硫酸混和后共热,能闻到一种香味,说明甲酸具有
(6)在甲酸溶液中加入氢氧化铜,能看到溶液变蓝色,说明甲酸具有______
(7)在新制氢氧化铜中加入甲酸溶液,加热看到有红色沉淀生成,说明甲酸具有______.
(1)实验室中利用乙醇在浓硫酸的作用下加热发生消去反应来制乙烯,原理方程式为:
CH3CH2OH
CH2═CH2↑+H2O,故答案为:CH3CH2OH
CH2═CH2↑+H2O;
(2)乙烯可以和氯化氢之间发生加成反应生成氯乙烷,原理方程式为:CH2═CH2+HCl
CH3CH2Cl,故答案为:CH2═CH2+HCl
CH3CH2Cl;
(3)在碳酸钠溶液中加入甲酸有二氧化碳气体放出,证明甲酸有酸性,酸性强于碳酸,故答案为:③;
(4)在甲酸钠晶体中加入浓磷酸,加热后放出能使湿润蓝色石蕊试纸变红的气体甲酸,说明甲酸具有挥发性,故答案为:①;
(5)甲酸与乙醇在浓硫酸的作用下加热会生成有香味的酯,故答案为:⑤;
(6)甲酸溶液和氢氧化铜之间发生中和反应,生成铜盐和水,说明甲酸具有酸性,故答案为:②;
(7)甲酸中含有醛基,具有还原性,能和氢氧化铜悬浊液反应生成砖红色沉淀,故答案为:④.
CH3CH2OH
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
(2)乙烯可以和氯化氢之间发生加成反应生成氯乙烷,原理方程式为:CH2═CH2+HCl
| 催化剂 |
| 催化剂 |
(3)在碳酸钠溶液中加入甲酸有二氧化碳气体放出,证明甲酸有酸性,酸性强于碳酸,故答案为:③;
(4)在甲酸钠晶体中加入浓磷酸,加热后放出能使湿润蓝色石蕊试纸变红的气体甲酸,说明甲酸具有挥发性,故答案为:①;
(5)甲酸与乙醇在浓硫酸的作用下加热会生成有香味的酯,故答案为:⑤;
(6)甲酸溶液和氢氧化铜之间发生中和反应,生成铜盐和水,说明甲酸具有酸性,故答案为:②;
(7)甲酸中含有醛基,具有还原性,能和氢氧化铜悬浊液反应生成砖红色沉淀,故答案为:④.

练习册系列答案
相关题目
 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.请按要求回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.请按要求回答下列问题:
(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:______.
(2)实验室用两种固体制取NH3的反应化学方程式为______.
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为______.
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为______.
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①焓变△H______0(填“>”、“<”或“=”).
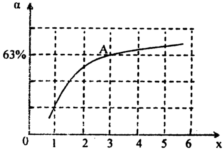
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)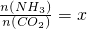 ,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是______.图中A点处,NH3的平衡转化率为______.
,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是______.图中A点处,NH3的平衡转化率为______.
(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)?2NH3(g),测得甲容器中H2的平衡转化率为40%.
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是______(填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为______.
 (2013?河西区一模)肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.请按要求回答下列问题:
(2013?河西区一模)肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.请按要求回答下列问题:
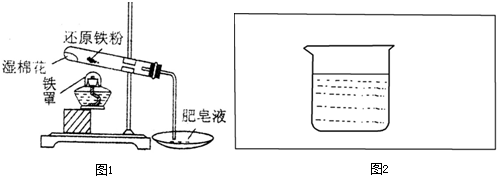
 ”表示),设计一套原电池装置,并验证有电流产生,请帮他在图2方框内补充全装置简图(要求标注正、负极及其材料和电解质溶液名称).
”表示),设计一套原电池装置,并验证有电流产生,请帮他在图2方框内补充全装置简图(要求标注正、负极及其材料和电解质溶液名称).