题目内容
4.下列说法错误的是( )| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 用铂丝蘸取某溶液置于酒精灯火焰上灼烧,直接观察火焰颜色,检验K+的存在 | |
| C. | 少量的钠保存在煤油中 | |
| D. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
分析 A.氯气和水反应生成盐酸和次氯酸,碱性条件下氯气更易溶于水;
B.钾元素焰色反应必须透过蓝色钴玻璃观察;
C.钠的密度大于水,且钠和煤油不反应;
D.分液操作为,分液漏斗中下层液体从下口放出,为防止引入杂质,上层液体从上口倒出.
解答 解:A.氯气和水反应生成盐酸和次氯酸,碱性条件下氯气更易溶于水,所以有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场,故A正确;
B.钾元素焰色反应必须透过蓝色钴玻璃观察,滤去黄光的干扰,故B错误;
C.钠的密度大于水,且钠和煤油不反应,所以钠储存在煤油中能隔绝空气和水,故C正确;
D.分液操作为,分液漏斗中下层液体从下口放出,为防止引入杂质,上层液体从上口倒出,否则易掺入杂质,故D正确;
故选B.
点评 本题考查基本操作及物质性质,为高频考点,明确实验原理及物质性质即可解答,易错选项是B,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
12.下列氧化反应属于吸热反应的是( )
| A. | 二氧化碳与赤热的炭反应生成一氧化碳 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 锌粒与稀H2SO4反应制取H2 | |
| D. | Ba(OH)2•8H2O与NH4Cl反应 |
19.有关能量的判断或表示方法正确的是( )
| A. | 由H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 | |
| C. | 2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2 H2O(l)△H=-285.8kJ/mol | |
| D. | 从C(石墨)=C(金刚石)△H=+1.9kJ/mol,可知石墨比金刚石更稳定 |
9.下列化合物中同分异构体数目最多的是( )
| A. | 戊烷 | B. | 戊烯 | C. | 戊醇 | D. | 戊酸 |
16.用下列实验装置进行实验,能达到相应实验目的是( )
| A. | 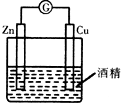 形成原电池 | B. | 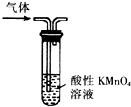 除去乙烯中混有的SO2 | ||
| C. | 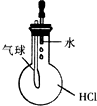 验证HCl气体在水中的溶解性 | D. | 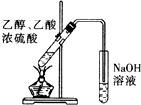 实验室制取乙酸乙酯 |
13.在反应A(s)+B(g)═2C(g)中,可使反应速率增大的措施是( )
①升高温度②降低压强③通入B气体④增加A的量⑤将块状固体A磨成粉末.
①升高温度②降低压强③通入B气体④增加A的量⑤将块状固体A磨成粉末.
| A. | ①③⑤ | B. | ①②④ | C. | ①④⑤ | D. | ①②③④⑤ |