题目内容
【题目】碘量法测定废水中硫化物的实验装置如图所示。
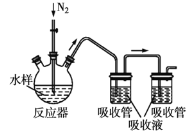
Ⅰ.取样、吹气、固硫
按右图连接好装置,检查气密性。取足量的醋酸锌吸收液于两支吸收管中,取100mL水样于反应器中,通入氮气一段时间后,向反应器中加入10mL盐酸,![]() 加热,反应后继续通入氮气。
加热,反应后继续通入氮气。
已知:废水中的硫化物在酸性条件下易转化为剧毒的硫化氢,醋酸锌可用于完全吸收硫化氢生成硫化锌沉淀。回答下列问题:
(1)图中反应器的名称是________,反应后继续通入氮气的目的是________,反应器加热温度不能高于![]() 的原因是________。
的原因是________。
Ⅱ.滴定、分析
关闭氮气后,往两支吸收管中各加入![]() 的碘标准溶液50mL(过量),静置。加入淀粉指示液,用
的碘标准溶液50mL(过量),静置。加入淀粉指示液,用![]() 的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定,共消耗
的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定,共消耗![]() ,溶液
,溶液![]() 。
。
(2)加入碘标准溶液时吸收管中发生反应的化学方程式为________。
(3)滴定终点的现象为________。
(4)废水中硫的含量为________![]() 。若只使用一支吸收管,可能致测定结果偏________(填“高”或“低”。)
。若只使用一支吸收管,可能致测定结果偏________(填“高”或“低”。)
【答案】三颈烧瓶(或三口烧瓶) 将硫化氢鼓入吸收管中以便完全吸收 温度太高,硫化氢逸出速率过快,导致不能被完全吸收 ![]() 当滴入最后一滴硫代硫酸钠溶液,溶液由蓝色变成无色,且半分钟内不恢复原色 32 低
当滴入最后一滴硫代硫酸钠溶液,溶液由蓝色变成无色,且半分钟内不恢复原色 32 低
【解析】
根据实验装置图和实验步骤分析解答(1)~(3);
(4)实验过程中涉及的反应为ZnS+I2=ZnI2+S、2S2O32-+I2═2I-+S4O62-,结合S原子守恒及电子守恒可知存在S~ZnS~I2,由2S2O32-+I2═2I-+S4O62-可计算剩余的碘据此分析解答。
(1)根据图示,图中反应器的名称是三颈烧瓶,反应后继续通入氮气的目的是将硫化氢全部吹入吸收管中以便完全反应,温度太高,硫化氢逸出速率过快,导致不能被完全吸收,因此反应器加热温度不能高于80℃,故答案为:三颈烧瓶;将硫化氢鼓入吸收管中以便完全反应;温度太高,硫化氢逸出速率过快,导致不能被完全吸收;
(2)加入碘标准溶液时,在吸收管中将ZnS氧化,反应的化学方程式为ZnS+I2=S+ZnI2,故答案为:ZnS+I2=S+ZnI2;
(3)根据反应方程式2S2O32-+I2═2I-+S4O62-和选用的指示剂淀粉溶液可知,滴定终点时,当滴入最后一滴Na2S2O3溶液,溶液由蓝色变为无色,且半分钟内不恢复原色,故答案为:当滴入最后一滴Na2S2O3溶液,溶液由蓝色变为无色,且半分钟内不恢复原色;
(4)n(I2)=0.05L×0.010molL-1=0.0005mol,由2S2O32-+I2═2I-+S4O62-可知吸收后剩余的碘为0.08L×0.010molL-1×![]() =0.0004mol,由S~ZnS~I2可知废水中硫的含量为
=0.0004mol,由S~ZnS~I2可知废水中硫的含量为![]() =32mgL-1,使用两个吸管,可保证硫化氢完全被吸收,若只使用一个吸收管,会导致测定结果偏低,故答案为:32;低。
=32mgL-1,使用两个吸管,可保证硫化氢完全被吸收,若只使用一个吸收管,会导致测定结果偏低,故答案为:32;低。

 科学实验活动册系列答案
科学实验活动册系列答案【题目】I.氮和氮的化合物在国防、工农业生产和生活中都有极其广泛的用途。请回答下列问题:
(1)亚硝酰氯(结构式为![]() )是有机合成中的重要试剂,它可由
)是有机合成中的重要试剂,它可由![]() 和
和![]() 在常温常压条件下反应制得,反应方程式为:
在常温常压条件下反应制得,反应方程式为:![]() 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:
化学键 |
|
|
|
|
键能 | 243 | 200 | 607 | 630 |
则![]()
![]() ________
________![]() 。
。
(2)在一个恒容密闭容器中充入![]() 和
和![]() 发生(1)中的反应,在温度分别为
发生(1)中的反应,在温度分别为![]() ℃、
℃、![]() ℃时测得
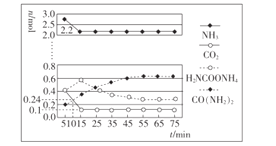
℃时测得![]() 的物质的量(单位:mol)与时间的关系如下表所示:
的物质的量(单位:mol)与时间的关系如下表所示:
t/min 温度 | 0 | 5 | 8 | 13 |
| 2 | 1.5 | 1.3 | 1.0 |
| 2 | 1.15 | 1.0 | 1.0 |
①![]() ________
________![]() (填“
(填“![]() ”“
”“![]() ”或“
”或“![]() ”)。
”)。
②温度为![]() 时,起始时容器内的压强为
时,起始时容器内的压强为![]() ,则该反应的平衡常数
,则该反应的平衡常数![]() ________(用平衡分压代替平衡浓度计算,分压
________(用平衡分压代替平衡浓度计算,分压![]() 总压
总压![]() 物质的量分数)(化为最简式)。
物质的量分数)(化为最简式)。
(3)近年来,地下水中的氮污染已成为世界性的环境问题。在金属![]() 、
、![]() 和依(
和依(![]() )的催化作用下,
)的催化作用下,![]() 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮(![]() ),其工作原理如图所示。
),其工作原理如图所示。
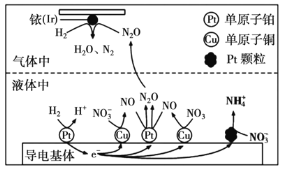
①![]() 表面发生反应的化学方程式为:________。
表面发生反应的化学方程式为:________。
②若导电基体上的![]() 颗粒增多,造成的后果是________。
颗粒增多,造成的后果是________。
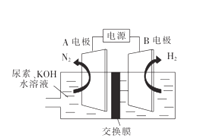
Ⅱ.利用电化学原理,将![]() 、
、![]() 和熔融
和熔融![]() 制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
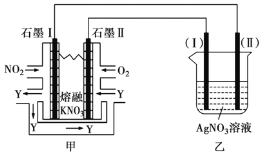
(4)①甲池工作时,![]() 转变成绿色硝化剂
转变成绿色硝化剂![]() ,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为________。
,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为________。
②若用10A的电流电解50min后,乙中阴极得到![]() ,则该电解池的电解效率为________%。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为
,则该电解池的电解效率为________%。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为![]() )
)