题目内容
已知:X、Y、Z、R四种短周期元素原子序数依次增大,X的气态氢化物水溶液呈碱性,Y原子的L层电子数是K层电子数的3倍,Z和R的单质在一定条件下与铜反应生成Cu2Z和CuR2,请根据要求填空。
(1)画出X的原子结构示意图 。R最高价氧化物对应水化物的化学式为 。
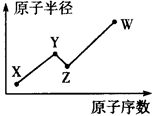
(2)Y、Z、R三种元素中原子半径最大的是 (用元素符号表示)。
(3)X气态氢化物与Z的最高价氧化物对应水化物反应生成的产物中所含化学键的类型为 ;检验该产物中阳离子的实验方法是 。
(4)R的单质通入到澄清石灰水中反应的离子方程式为 。
(1)画出X的原子结构示意图 。R最高价氧化物对应水化物的化学式为 。
(2)Y、Z、R三种元素中原子半径最大的是 (用元素符号表示)。
(3)X气态氢化物与Z的最高价氧化物对应水化物反应生成的产物中所含化学键的类型为 ;检验该产物中阳离子的实验方法是 。
(4)R的单质通入到澄清石灰水中反应的离子方程式为 。
(1)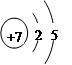 ;HClO4 (2)S。 (3)离子键、共价键、配位键;
;HClO4 (2)S。 (3)离子键、共价键、配位键;
取少量产物于试管中,加入浓的氢氧化钠溶液,将粘有湿润的红色石蕊试纸的玻璃棒放在试管口部(或将蘸有浓盐酸的玻璃棒放在试管口部),加热,若试纸变蓝(或若有白烟生成),则证明产物中含有NH4+。
(4)Cl2+2OH-=Cl-+ClO-+H2O。
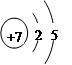 ;HClO4 (2)S。 (3)离子键、共价键、配位键;
;HClO4 (2)S。 (3)离子键、共价键、配位键;取少量产物于试管中,加入浓的氢氧化钠溶液,将粘有湿润的红色石蕊试纸的玻璃棒放在试管口部(或将蘸有浓盐酸的玻璃棒放在试管口部),加热,若试纸变蓝(或若有白烟生成),则证明产物中含有NH4+。
(4)Cl2+2OH-=Cl-+ClO-+H2O。
。
试题分析:(1)X是短周期元素X的气态氢化物水溶液呈碱性,则X是N元素。Y原子的L层电子数是K层电子数的3倍,Y是O元素。Z和R的单质在一定条件下与铜反应生成Cu2Z和CuR2,则Z是元素,R是Cl元素。Cl元素最高价氧化物对应水化物是高氯酸,它的的化学式为HClO4。2)氮元素是第二周期的元素,硫、氯是第三周期的元素。对于不同周期的元素来说,原子核外电子层数越多,原子半径越大。对于电子层数相同的元素来说,原子序数越大,原子半径越小。所以三者半径最大的是硫元素。(3)X气态氢化物是NH3与Z的最高价氧化物对应水化物是HClO4。反应生成的产物NH4ClO4。中所含化学键有离子键、共价键、配位键;检验NH4+方法向待检验溶液中加入浓的氢氧化钠溶液,并加热,若产生能使紫色石蕊试液变蓝的气体就证明含有铵根离子。或者将粘有湿润的红色石蕊试纸的玻璃棒放在试管口部(或将蘸有浓盐酸的玻璃棒放在试管口部),加热,若试纸变蓝(或若有白烟生成),则证明产物中含有NH4(4)Cl2与氢氧化钙溶液发生反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O。
试题分析:(1)X是短周期元素X的气态氢化物水溶液呈碱性,则X是N元素。Y原子的L层电子数是K层电子数的3倍,Y是O元素。Z和R的单质在一定条件下与铜反应生成Cu2Z和CuR2,则Z是元素,R是Cl元素。Cl元素最高价氧化物对应水化物是高氯酸,它的的化学式为HClO4。2)氮元素是第二周期的元素,硫、氯是第三周期的元素。对于不同周期的元素来说,原子核外电子层数越多,原子半径越大。对于电子层数相同的元素来说,原子序数越大,原子半径越小。所以三者半径最大的是硫元素。(3)X气态氢化物是NH3与Z的最高价氧化物对应水化物是HClO4。反应生成的产物NH4ClO4。中所含化学键有离子键、共价键、配位键;检验NH4+方法向待检验溶液中加入浓的氢氧化钠溶液,并加热,若产生能使紫色石蕊试液变蓝的气体就证明含有铵根离子。或者将粘有湿润的红色石蕊试纸的玻璃棒放在试管口部(或将蘸有浓盐酸的玻璃棒放在试管口部),加热,若试纸变蓝(或若有白烟生成),则证明产物中含有NH4(4)Cl2与氢氧化钙溶液发生反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O。

练习册系列答案
相关题目