题目内容
16.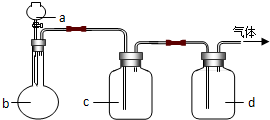 拟用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c.d表示相应仪器中加入的试剂).下列可以得到干燥纯净的气体的选项是( )
拟用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c.d表示相应仪器中加入的试剂).下列可以得到干燥纯净的气体的选项是( )| 选项 | 气体 | a | b | c | d |
| A | CO2 | 盐酸 | CaCO3 | 饱和Na2CO3溶液 | 浓硫酸 |
| B | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
| C | Cl2 | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 浓硫酸 |
| D | NO2 | 浓HNO3 | 铜屑 | H2O | 固体NaOH |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化碳能够与碳酸钠反应生成碳酸氢钠,应该用饱和碳酸氢钠溶液除去HCl;
B.氨气极易溶于水,c中不能用水,否则无法获得氨气;
C.二氧化锰与浓盐酸在加热条件下反应生成氯气,氯气不溶于饱和氯化钠溶液,可用饱和氯化钠溶液除去氯气中的氯化氢,然后用浓硫酸干燥氯气;
D.生成的二氧化氮在c中与水反应生成NO气体,无法获得二氧化氮.
解答 解:A.制取的二氧化碳中混有HCl,由于二氧化碳与碳酸钠溶液反应,应该用饱和碳酸氢钠溶液除去二氧化碳中的HCl,故A错误;
B.氨气极易溶于水,c中盛有水,在d中不会获得氨气,故B错误;
C.在加热条件下,浓盐酸与二氧化锰反应生成氯气,生成的氯气中混有氯化氢,需要用饱和氯化钠溶液除去,然后用浓硫酸干燥氯气,该方法可以获得干燥、纯净的氯气,故C正确;
D.铜与浓硝酸反应生成二氧化氮气体,二氧化氮与水反应生成NO气体,最终得到的是NO,无法获得二氧化氮,故D错误;
故选C.
点评 本题考查了实验装置的综合应用,题目难度中等,明确常见气体的性质及制备原理为解答关键,注意常见装置的组合方法及使用方法,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
7.下列化合物中,既显酸性,又能发生酯化反应和消去反应的是( )
| A. |  | B. | 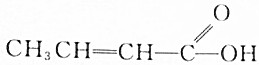 | ||
| C. | 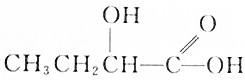 | D. | 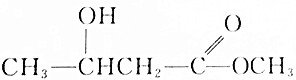 |
8.相同温度下,体积均为1.5L的两个恒容容器中发生可逆反应:X2(g)+3Y2(g)═2XY3(g)△H=-92.6kJ•mol-1,实验测得有关数据如下表:
下列叙述不正确的是( )
| 容器 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
| A. | 容器①中达到平衡时,Y2的转化率为50% | |
| B. | Q=27.78 kJ | |
| C. | 相同温度下;起始时向容器中充入1.0 X2 mol、3.0 mol Y2和2 mol XY3;反应达到平衡前v(正)>v(逆) | |
| D. | 容器①、②中反应的平衡常数相等,K=$\frac{16}{27}$ |
5.PH3是一种无色、有剧毒的气体,其分子结构和NH3相似,下列判断正确的是( )
| A. | N-H的键长比P-H的键长短,所以PH3的沸点比NH3低 | |
| B. | PH3分子的立体构型是三角锥形,与NH3互为等电子体 | |
| C. | PH3分子是极性分子,极易溶于水,因为它与水分子间存在氢键 | |
| D. | NH3比PH3稳定,因为NH3分子间存在氢键 |
6. 物质A~E在水中电离产生下列离子:
物质A~E在水中电离产生下列离子:
常温下将各物质的溶液从1ml稀释到1000ml,PH的变化关系如图所示,期中A和D反应生成E.请回答下列问题
(1)根据PH的变化关系,写出下列物质的化学式:BNaOH DCH3COOH
(2)写出A与C反应的离子方程式NH3+H+=NH4+
(3)25℃时0.1mol/L的NH4Cl溶液的PH=a,则NH4Cl溶液中c(H+)-c(NH3•H2O)=c(OH-)(用含a的关系式表示)
(4)H2SO4的酸式盐NH4HSO4,在NH4HSO4溶液中加入NaOH使溶液呈中性,则溶液中各离子浓度大小顺序为C(Na+)>C(SO42-)>C(NH4+)>C(H+)=C(OH-).
 物质A~E在水中电离产生下列离子:
物质A~E在水中电离产生下列离子:| 阳离子 | NH4+ H+ Na+ |
| 阴离子 | OH-CH3COO- SO42- |
(1)根据PH的变化关系,写出下列物质的化学式:BNaOH DCH3COOH
(2)写出A与C反应的离子方程式NH3+H+=NH4+
(3)25℃时0.1mol/L的NH4Cl溶液的PH=a,则NH4Cl溶液中c(H+)-c(NH3•H2O)=c(OH-)(用含a的关系式表示)
(4)H2SO4的酸式盐NH4HSO4,在NH4HSO4溶液中加入NaOH使溶液呈中性,则溶液中各离子浓度大小顺序为C(Na+)>C(SO42-)>C(NH4+)>C(H+)=C(OH-).
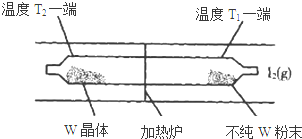 利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0.
利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0.