题目内容
10. (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小.(填一定增大、一定减小、或可能增大也可能减小);
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小.(填一定增大、一定减小、或可能增大也可能减小);(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)═CO2(g)+H2 (g)△H<0.
CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1.
(3)该反应的化学平衡常数表达式为K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$,850℃时当反应进行到4min时即达到平衡状态,这时化学平衡常数的数值为1.
分析 (1)化平衡常数K值越大,表示可逆反应正向进行程度越大;温度升高,若平衡正向移动,平衡常数增大,若平衡逆向移动,平衡常数减小;
(2)由图可知,0~4min内△c(CO)=(0.2-0.08)mol/L=0.12mol/L,根据v=$\frac{△c}{△t}$计算v(CO);
(3)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
850℃时当反应进行到4min时即达到平衡状态,平衡时c(CO)=0.08mol/L,c(H2O)=0.18mol/L,由方程式可知c(CO2)=c(H2)=△c(CO)=(0.2-0.08)mol/L=0.12mol/L,代入平衡常数表达式计算.
解答 解:(1)化平衡常数K值越大,表示可逆反应正向进行程度越大;温度升高,若平衡正向移动,平衡常数增大,若平衡逆向移动,平衡常数减小,故升高温度平衡常数可能增大也可能减小,
故答案为:可逆反应的进行程度越大;可能增大也可能减小;
(2)由图可知,0~4min内△c(CO)=(0.2-0.08)mol/L=0.12mol/L,故v(CO)=$\frac{0.12mol/L}{4min}$=0.03mol/(L.min),
故答案为:0.03;
(3)CO(g)+H2O(g)═CO2(g)+H2 的化学平衡常数表达式K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$;
850℃时当反应进行到4min时即达到平衡状态,平衡时c(CO)=0.08mol/L,c(H2O)=0.18mol/L,由方程式可知c(CO2)=c(H2)=△c(CO)=(0.2-0.08)mol/L=0.12mol/L,故850℃时平衡常数K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$=$\frac{0.12×0.12}{0.08×0.18}$=1,
故答案为:$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$;1.
点评 本题考查化学平衡常数及有关计算、反应速率计算等,难度不大,侧重对基础知识的巩固.

| A. | 在海轮船壳上镶入锌块保护海轮,利用的是牺牲阳极的阴极保护法 | |
| B. | 加入合适的催化剂,能降低反应活化能,从而改变反应的焓变 | |
| C. | 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 | |
| D. | 稀醋酸中加入少量CH3COONa固体,醋酸的电离程度减小,c(CH3COO-)增大 |
| 元素 | 有关信息 |
| X | 元素主要常见化合价为-2和-1价,原子半径为0.074nm. |
| Y | 所在主族序数与所在周期序数之差为4. |
| Z | 原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其气态氢化物与Y单质发生反应生成淡黄色固体. |
| D | 最高价氧化物对应的水化物,能电离出离子数、电子数都相等的阴、阳离子. |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏. |
| F | 元素所在的主族序数等于周期序数. |
(1)Z在周期表中的位置第三周期第ⅥA族,D的最高价氧化物对应水化物的电子式为

(2)X单质与D单质反应生成的D2X2能和H2O反应,写出其离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑.
(3)E元素与Y元素可形成EY2和EY3两种化合物,向淀粉碘化钾溶液滴加几滴EY3的浓溶液,原无色溶液可变为紫色,其原因是2Fe3++2I-═2Fe2++I2(用离子方程式表示).
(4)E单质在发生吸氧腐蚀时的正极反应方程式O2+2H2O+4e-═4OH-
(5)F的一种复盐常用作净水剂,用离子方程式表示其净水原理Al3++3H2O═Al(OH)3(胶体)+3H+.
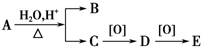 其中B与E互为同分异构体,则A可能的结构有( )
其中B与E互为同分异构体,则A可能的结构有( )| A. | 8种 | B. | 4种 | C. | 2种 | D. | 1种 |
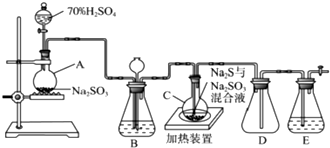
 某兴趣小组采用如图装置制取并探究SO2气体的性质.
某兴趣小组采用如图装置制取并探究SO2气体的性质.