题目内容
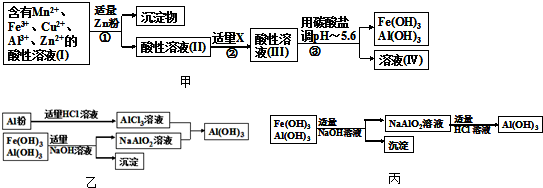
将AlCl3溶液和NaAlO2溶液分别蒸发并灼烧,所得产物的主要成份是
- A.均为Al(OH)3
- B.前者得Al2O3,后者得NaAlO2
- C.均为Al2O3
- D.前者得AlCl3,后者得NaAlO2
B
分析:AlCl3溶液在加热时水解生成Al(OH)3,Al(OH)3在加热条件下分解生成Al2O3.NaAlO2溶液加入水解生成Al(OH)3与NaOH,最终又反应生成NaAlO2.
解答:AlCl3溶液在加热时水解生成Al(OH)3,生成的HCl易挥发,最终生成Al(OH)3,在加强热时,Al(OH)3不稳定,分解生成Al2O3;
NaAlO2溶液加入水解生成Al(OH)3与NaOH,最终又反应生成NaAlO2,NaAlO2溶液蒸发并灼烧得到NaAlO2.
故选B.
点评:本题考查铝的化合物性质、盐类水解的应用,题目难度不大,注意把握水解的原理及应用.
分析:AlCl3溶液在加热时水解生成Al(OH)3,Al(OH)3在加热条件下分解生成Al2O3.NaAlO2溶液加入水解生成Al(OH)3与NaOH,最终又反应生成NaAlO2.
解答:AlCl3溶液在加热时水解生成Al(OH)3,生成的HCl易挥发,最终生成Al(OH)3,在加强热时,Al(OH)3不稳定,分解生成Al2O3;
NaAlO2溶液加入水解生成Al(OH)3与NaOH,最终又反应生成NaAlO2,NaAlO2溶液蒸发并灼烧得到NaAlO2.
故选B.
点评:本题考查铝的化合物性质、盐类水解的应用,题目难度不大,注意把握水解的原理及应用.

练习册系列答案
相关题目
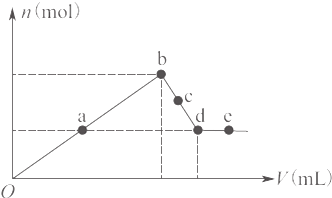 向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )
向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )| A、a、c两点沉淀物成分相同,d、e两点沉淀物成分相同 | B、在反应过程中,各状态点溶液的pH大小顺序是:e>d>c>a>b | C、b-c段与c-d段溶液中阴离子的物质的量相等 | D、在d点,向溶液中逐滴加入盐酸,沉淀量将减少 |