题目内容
实验室用浓硫酸制氯化氢气体是因为浓硫酸是
- A.强酸
- B.干燥剂
- C.脱水剂
- D.难挥发性强酸

化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空
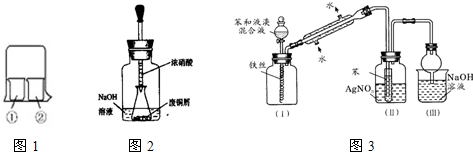
(1)实验室经常用烧杯进行性质实验研究,如图所示装置及下表中试剂,过一段时间

|
实验编号 |
①中的物质 |
②中的物质 |
|
1 |
淀粉碘化钾溶液 |
浓硝酸 |
|
2 |
酚酞溶液 |
浓硫酸 |
|
3 |
氯化铝溶液 |
浓氨水 |
|
4 |
湿润的红纸 |
饱和氯水 |
实验1、2、3、4烧杯①中的现象分别是 , , , ,
(2)用下图装置:废铜屑制硝酸铜,反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____(填写化学式)

(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题.

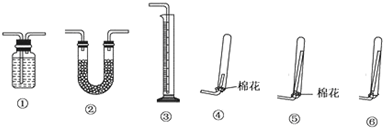
①若要测定生成的NH3的体积,则必须选择的装置是 (填装置序号),装置中所盛试剂应具有的性质是 .收集干燥的NH3,收集装置应选择(填装置序号) ,理由是 .
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1—10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式 。
(4)下图是苯与溴发生反应并进行产物检验的反应装置
实验装置中的冷凝管“左低右高”的放置目的是____________,整套实验装置中能防止倒吸的装置是______________(填装置序号)
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫。
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠。
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠。
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎。
②将研钵中的样品露置在空气中两天。
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡。
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少。
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)_____________。
(6)如果要验证③是否成立的实验方法是______________________
化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空
(1)实验室经常用烧杯进行性质实验研究,如用图1所示装置及下表中试剂,过一段时间实验1、2、3、4烧杯①中的现象分别是______,______,______,______,
| 实验编号 | ①中的物质 | ②中的物质 |
| 1 | 淀粉碘化钾溶液 | 浓硝酸 |
| 2 | 酚酞溶液 | 浓硫酸 |
| 3 | 氯化铝溶液 | 浓氨水 |
| 4 | 湿润的红纸 | 饱和氯水 |
(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题.

①若要测定生成的NH3的体积,则必须选择的装置是______(填装置序号),装置中所盛试剂应具有的性质是______.收集干燥的NH3,收集装置应选择(填装置序号)______,理由是______.
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1-10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式______.
(4)图3是苯与溴发生反应并进行产物检验的反应装置实验装置中的冷凝管“左低右高”的放置目的是______,整套实验装置中能防止倒吸的装置是______(填装置序号)
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫.
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠.
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠.
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎.
②将研钵中的样品露置在空气中两天.
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡.
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少.
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)______.
(6)如果要验证③是否成立的实验方法是______.