题目内容
【题目】我国利用合成气直接制烯烃获重大突破,其原理是
反应①:C(s)+1/2O2(g) = CO(g) ΔH1
反应②:C(s)+H2O(g) = CO(g)+H2(g) ΔH2
反应③:CO(g)+2H2(g) = CH3OH(g) ΔH3=-90.1 kJ·mol-1
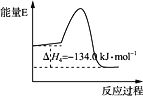
反应④:2CH3OH(g) = CH3OCH3(g)+H2O(g) ΔH4,能量变化如图所示
反应⑤:3CH3OH(g)= CH3CH=CH2(g)+3H2O(g) ΔH5=-31.0 kJ·mol-1
下列说法正确的是
A. 反应③使用催化剂,ΔH3减小
B. 反应④中正反应的活化能大于逆反应的活化能
C. ΔH1-ΔH2<0
D. 反应①和反应②,制取等量的CO,无论哪种途径,消耗的能量均相同
【答案】C
【解析】分析:A.使用催化剂不能改变反应热;B.④为放热反应,正反应的活化能小于逆反应的活化能;C. ①-②得H2(g)+1/2O2(g)=H2O(g),氢气燃烧放出热量;D. 反应①为放热反应,反应②为吸热反应。
详解:A. 催化剂可以降低反应的活化能,但不改变反应热,则反应③使用催化剂,ΔH3不变,故A错误;
B. ④为放热反应,焓变为正逆反应的活化能之差,则反应④中正反应的活化能小于逆反应的活化能,故B错误;
C. ①-②得H2(g)+1/2O2(g)=H2O(g),氢气燃烧放出热量,则ΔH1-ΔH2<0,故C正确;
D. 反应①为放热反应,反应②为吸热反应,制取等量的CO时,反应①释放能量,反应②消耗能量,故D错误;答案选C。

练习册系列答案
相关题目