题目内容
【题目】以苯为主要原料,制取高分子材料N和R的流程如下:

已知: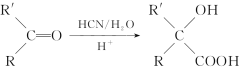
(1)B中含氧官能团的名称是________。
(2)由![]() 生成
生成![]() 的反应类型是________。
的反应类型是________。
(3)反应Ⅰ的反应条件是________。
(4)化合物C的结构简式是________。
(5)反应Ⅱ的化学反应方程式是________。
(6)下列说法正确的是________(填字母)。
a.A可与NaOH溶液反应
b.常温下,A能和水以任意比混溶
c.化合物C可使酸性高锰酸钾溶液褪色
d.E存在顺反异构体
(7)反应Ⅲ的化学反应方程式是________。
(8)符合下列条件的B的同分异构体有________种。
a.能与饱和溴水反应生成白色沉淀
b.属于酯类
c.苯环上只有两个对位取代基
【答案】(1)羟基、羧基 (2)取代反应
(3)NaOH水溶液加热后酸化
(4)![]()

(6)a、c
(7)
(8)6
【解析】(1)由题干已知 ,可知B为
,可知B为 ,B中含氧官能团的名称是羟基、羧基。
,B中含氧官能团的名称是羟基、羧基。
(2)由![]() 生成
生成![]() 的反应类型是苯环上的取代反应。(3)目标产物中有酚羟基,应为卤代烃的水解反应,故反应条件是NaOH水溶液加热后酸化。(4)A与C反应生成N,是酚醛缩合反应,故C应为醛类物质,则C的结构简式是
的反应类型是苯环上的取代反应。(3)目标产物中有酚羟基,应为卤代烃的水解反应,故反应条件是NaOH水溶液加热后酸化。(4)A与C反应生成N,是酚醛缩合反应,故C应为醛类物质,则C的结构简式是![]() 。(5)反应Ⅱ是酯化反应,化学反应方程式是
。(5)反应Ⅱ是酯化反应,化学反应方程式是
 。
。
(6)A是苯酚,可与NaOH溶液反应,a正确;常温下,苯酚在水中的溶解度很小,b错误;化合物C是![]() ,既是碳碳双键,又有醛基,可使酸性高锰酸钾溶液褪色,c正确;D生成E是消去反应,E的结构简式为
,既是碳碳双键,又有醛基,可使酸性高锰酸钾溶液褪色,c正确;D生成E是消去反应,E的结构简式为![]() ,不存在顺反异构体,d错误。
,不存在顺反异构体,d错误。
(7)E到R是加聚反应,化学反应方程式是n 。
。
(8)符合条件的B( )的同分异构体有
)的同分异构体有


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】下列对晶体类型判断正确的是( )
选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
A. A B. B C. C D. D