��Ŀ����
����Ŀ��C��NaMO2����ǿ�ѧ�������з��������ӵ�أ���Ϥ�õ�ؿ��Խ���ͳ﮵�ص�������������7�����õ�صĵ�ط�ӦʽΪ��NaMO2+nCNa��1��x��MO2+NaxCn �� �����йظõ�ص�˵����ȷ���ǣ������� 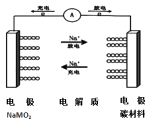
A.��طŵ�ʱ����Һ�����������ƶ�
B.��س��ʱ��������ӦʽΪ��nC+x Na+��xe���TNaxCn
C.������ͬ��������ʱ������������������ӵ����ʵ���������ʱ��
D.�õ�ظ����ĵ缫��ӦΪ��NaMO2��xe���TNa��1��x��MO2+xNa+
���𰸡�D
���������⣺A����طŵ�ʱ����ԭ��صĹ���ԭ����ԭ����У�������е����������������������������������ƶ�����A����
B����س��ʱ���ǵ���װ�õĹ���ԭ���������Ϸ���ʧ���ӵ�������Ӧ���缫��ӦʽΪNaxCn��xe���TnC+x Na+����B����
C����Na��Ħ������Ϊ23g/mol���� ![]() ��ʧȥ�ĵ�������֪��������ͬ��������ʱ�����������ʱ���������ӵ����ʵ������ƶ࣬��C����
��ʧȥ�ĵ�������֪��������ͬ��������ʱ�����������ʱ���������ӵ����ʵ������ƶ࣬��C����
D����طŵ�ʱ����������ʧ���ӵ�������Ӧ����NaMO2��xe���TNa��1��x��MO2+xNa+����D��ȷ��
��ѡ��D��

��ϰ��ϵ�д�
�����Ŀ