题目内容
在适当条件下,30mL由氮氢两种元素构成的气体NxHy完全分解生成30mL N2和60mL H2(同温同压下测定),则NxHy的摩尔质量为( )
| A、16 g?mol-1 | B、17 g?mol-1 | C、32 g?mol-1 | D、34g?mol-1 |
分析:在化学反应中,各气体的体积之比等于各物质的计量系数比,根据原子守恒来解答.
解答:解:各气体的体积之比=各物质的计量系数比=30:30:60=1:1:2,所以反应表达为:NxHy=N2+2H2,根据原子个数守恒,NxHy为N2H4,
摩尔质量为:(14×2+1×4)g/mol=32g/mol,故选C.
摩尔质量为:(14×2+1×4)g/mol=32g/mol,故选C.
点评:本题考查了摩尔质量的概念和阿伏加德罗定律,较简单.要明确化学反应中,各气体的体积之比等于各物质的计量系数比之一结论以及原子守恒思想在反应中的应用知识.

练习册系列答案
相关题目
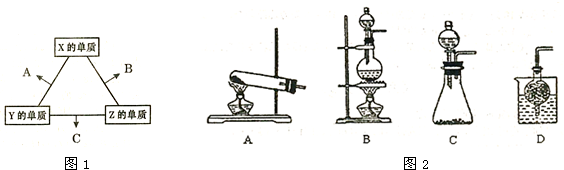
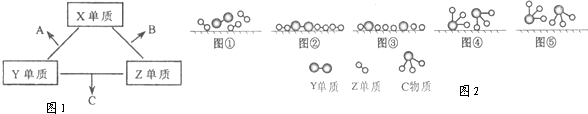
 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化: 4NO+6H2O
4NO+6H2O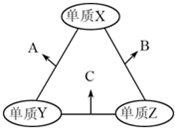 (2013?普陀区二模)有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16.三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子.有关判断不正确的是( )
(2013?普陀区二模)有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16.三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子.有关判断不正确的是( )