题目内容
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.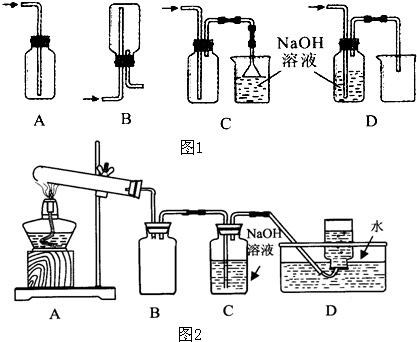
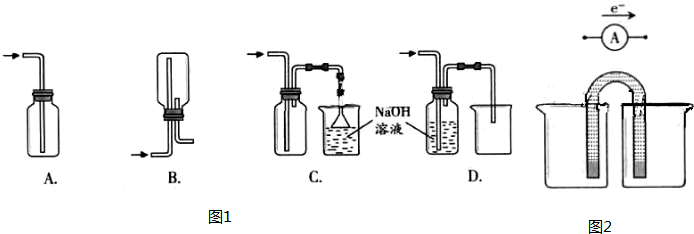
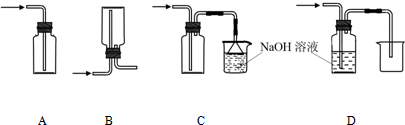
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验,如图1所示.
①写出该反应的离子方程式
②下列收集Cl2的装置正确装置是
③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是
④设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,
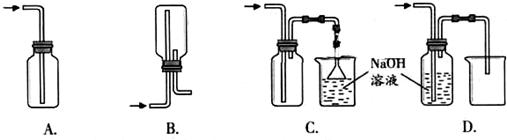
(2)某化学兴趣小组为了探究AgNO3的热稳定性,设计了如下实验.
用如图2所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束以后,试管中残留固体为黑色.
①装置B的作用是
②经小组讨论并验证该无色气体为O2,其验证方法是
【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】试管中残留的黑色固体可能是:ⅠAg;ⅡAg2O;ⅢAg和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,④该小组得出的AgNO3固体热分解的化学方程式为
分析:(1)①根据浓盐酸和二氧化锰的性质判断生成物,从而确定方程式;
②氯气是比空气重的可溶于水的气体,依据氯气物理性质和装置分析;
③氯气和水反应生成盐酸和次氯酸;依据平衡状态各物质性质分析判断;
④依据氯气具有氧化性能氧化溴离子为溴单质,溴单质在四氯化碳中溶解度大,据此现象分析判断设计实验;
(2)①装置中B为安全瓶防止倒吸;
②依据氧气助燃性检验;
③实验操作加入的试剂若是硝酸,固体溶解,银单质反应溶解,氧化银也能溶于硝酸;
④装置A加热AgNO3固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气体为氧气,依据实验a可知产物为银,氧化银溶于氨水.
②氯气是比空气重的可溶于水的气体,依据氯气物理性质和装置分析;
③氯气和水反应生成盐酸和次氯酸;依据平衡状态各物质性质分析判断;
④依据氯气具有氧化性能氧化溴离子为溴单质,溴单质在四氯化碳中溶解度大,据此现象分析判断设计实验;
(2)①装置中B为安全瓶防止倒吸;
②依据氧气助燃性检验;
③实验操作加入的试剂若是硝酸,固体溶解,银单质反应溶解,氧化银也能溶于硝酸;
④装置A加热AgNO3固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气体为氧气,依据实验a可知产物为银,氧化银溶于氨水.
解答:解:(1)①浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水,二氧化锰、氯气、水在离子反应中应保留化学式,离子反应方程式为:MnO2+2Cl-+4H+
Cl2↑+Mn2++2H2O,
故答案为:MnO2+2Cl-+4H+
Cl2↑+Mn2++2H2O;
②氯气是比空气中的可溶于水水的有毒气体;
A.导气管位置正确,因为氯气比空气重用向上排气方法,但只有进气口,无出气口,无法排出气体,故A错误;
B.此装置是用来收集比空气轻的气体,若收集氯气,需要短进长出,故B错误;
C.装置长进短出可以收集比空气重的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D.氯气通入NaOH溶液会发生反应.氯气被氢氧化钠吸收,不能收集到氯气,故D错误;
故答案为:C;
③将Cl2通入水中,发生反应Cl2+H2O?HCl+HClO,所得溶液中具有氧化性的含氯粒子为Cl2 HClO ClO-,故答案为:Cl2、HClO、ClO-;
④氯气具有氧化性能氧化溴离子为溴单质,溴单质在四氯化碳中溶解度大,所以可用胶头滴管向试管中滴加溴化钠溶液,充分振荡反应,Cl2+2Br-=2Cl-+Br2,静置后溴溶于下层的四氯化碳层呈橙色,
故答案为:用胶头滴管向试管中滴加溴化钠溶液、震荡使其充分反应,发现溶液出现分层现象,下层溶液变为橙色;
(2)①装置导气管略露出胶塞,是安全瓶,可以繁殖C装置中的液体到吸入发生装置A,故答案为:防止倒吸;
②氧气具有助燃性,用带火星的木条深入集气瓶中,木条复燃证明无色气为氧气,故答案为:用带火星的小木条插入集气瓶内,木条复燃,证明无色气体为O2;
③b实验加入的硝酸可以溶解Ag2O,也可以溶解Ag,不能检验固体成分,故答案为:b;
④实验a加入氨水,银不能溶解于氨水溶液,Ag2O能溶于氨水中形成银氨溶液,可以验证固体成分的判断,加入足量氨水,振荡黑色固体不溶解,说明生成的固体为Ag,装置A加热AgNO3固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气体为氧气,所以AgNO3固体热分解的产物有Ag、NO2、O2,方程式为:2AgNO3
2Ag+2NO2↑+O2↑,故答案为:2AgNO3
2Ag+2NO2↑+O2↑.
| ||
故答案为:MnO2+2Cl-+4H+
| ||
②氯气是比空气中的可溶于水水的有毒气体;
A.导气管位置正确,因为氯气比空气重用向上排气方法,但只有进气口,无出气口,无法排出气体,故A错误;
B.此装置是用来收集比空气轻的气体,若收集氯气,需要短进长出,故B错误;
C.装置长进短出可以收集比空气重的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D.氯气通入NaOH溶液会发生反应.氯气被氢氧化钠吸收,不能收集到氯气,故D错误;
故答案为:C;
③将Cl2通入水中,发生反应Cl2+H2O?HCl+HClO,所得溶液中具有氧化性的含氯粒子为Cl2 HClO ClO-,故答案为:Cl2、HClO、ClO-;
④氯气具有氧化性能氧化溴离子为溴单质,溴单质在四氯化碳中溶解度大,所以可用胶头滴管向试管中滴加溴化钠溶液,充分振荡反应,Cl2+2Br-=2Cl-+Br2,静置后溴溶于下层的四氯化碳层呈橙色,
故答案为:用胶头滴管向试管中滴加溴化钠溶液、震荡使其充分反应,发现溶液出现分层现象,下层溶液变为橙色;
(2)①装置导气管略露出胶塞,是安全瓶,可以繁殖C装置中的液体到吸入发生装置A,故答案为:防止倒吸;
②氧气具有助燃性,用带火星的木条深入集气瓶中,木条复燃证明无色气为氧气,故答案为:用带火星的小木条插入集气瓶内,木条复燃,证明无色气体为O2;
③b实验加入的硝酸可以溶解Ag2O,也可以溶解Ag,不能检验固体成分,故答案为:b;
④实验a加入氨水,银不能溶解于氨水溶液,Ag2O能溶于氨水中形成银氨溶液,可以验证固体成分的判断,加入足量氨水,振荡黑色固体不溶解,说明生成的固体为Ag,装置A加热AgNO3固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气体为氧气,所以AgNO3固体热分解的产物有Ag、NO2、O2,方程式为:2AgNO3
| ||
| ||
点评:本题考查了实验设计的方法和物质实验验证方案分析判断,掌握氯气、以及氯的化合物、硝酸银、硝酸等物质的性质是解题关键,题目难度中等.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目