题目内容
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O![]() Cu2O+H2↑
Cu2O+H2↑
(1)已知:①2Cu(s)+1/2O2(g)=Cu2O(s) △H=-169kJ/mol
②C(s)+1/2O2(g)=CO(g) △H=-110.5kJ/mol
③Cu(s)+1/2O2(g)=CuO(s) △H=-157kJ/mol
则方法a中反应的热化学方程式是:_________________。
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
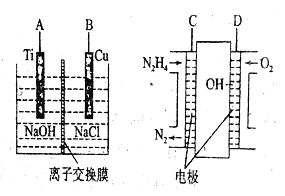
① 上述装置中B电极应连______电极(填“℃”或“D”)
② 该离子交换膜为_______离子交换膜(填“阴”或“阳”),该电解池的阳极反应式为:______。
③ 原电池中负极反应式为:_______________。
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:
2H2O![]() 2H2(g)+O2(g) △H>0
2H2(g)+O2(g) △H>0
水蒸气的浓度随时间t变化如下表所示:

①催化剂的效率:实验①_______实验②(填“>”或“<”);
② 实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:_______。
【答案】 2CuO(s)+C(s)=Cu2O(s)+CO(g) ΔH=+34. 5kJ/mol D 阴 2Cu-2e-+2OH-= Cu2O+H2O N2H4-4e—+4OH-=N2↑+4H2O < K1=K2<K3
【解析】(1)①2Cu(s)+ ![]() O2(g)═Cu2O(s)△H=-169kJmol-1;②C(s)+
O2(g)═Cu2O(s)△H=-169kJmol-1;②C(s)+ ![]() O2(g)═CO(g)△H=-110.5kJmol-1;③2Cu(s)+O2(g)═2CuO(s)△H=-314kJmol-1;
O2(g)═CO(g)△H=-110.5kJmol-1;③2Cu(s)+O2(g)═2CuO(s)△H=-314kJmol-1;
依据盖斯定律②+①-③得到:C(s)+2CuO (s)=CuO(s)+CO(g)△H=+34.5kJmol-1;
(2)①铜失电子发生氧化反应,为电解池的阳极,故B连接电源的正极,而燃烧电池通氧气的极为正极,则B连接D;
②电解池工作时,OH-向阳极移动,则离子交换膜为阴离子交换膜;在电解池中,当阳极是活泼电极时,该电机本身发生失电子得还原反应,在碱性环境下,金属铜失去电子的电极反应为2Cu-2e-+2OH-=Cu2O+H2O;
③原电池的负极发生氧化反应,其电极反应为 N2H4-4e—+4OH-=N2↑+4H2O;
(3)催化剂不会引起化学平衡状态的改变,会使反应速率加快,反应②比反应①达到平衡所用时间短,平衡状态相同,反应速率快,所以①<②,实验温度越高达到化学平衡时水蒸气转化率越大,②和③相比,③转化率高,所以T2>T1;平衡常数只受温度影响,且升高温度平衡正向移动,则实验①、②、③的化学平衡常数K1、K2、K3的大小关系为K1=K2<K3。

 阅读快车系列答案
阅读快车系列答案