��Ŀ����
������������������������Ź㷺��Ӧ��
��1�������ܽ���ˮ���õ�����Һ��Ϊ��ˮ�����ܽ���ˮʱ��ˮ������Ӧ����һˮ�ϰ���NH3?H2O��������һ�����д��һˮ�ϰ��ĵ��뷽��ʽ �����������뷽��ʽ��֪������ˮ�м���ϡ�������ɵ����� ���ѧʽ��
��2����״���£��� 2.24L�İ�������ˮ��� 0.5L��Һ��������Һ�����ʵ���Ũ��Ϊ mol/L��
��3��������Cl2��Ӧ����Ӧ����ʽ���£�8NH3+3Cl2�T6NH4Cl+N2�����ø÷�Ӧ��ԭ�����ڹ�ҵ�Ͽ����ڼ������������Ĺܵ��Ƿ�©�����÷�Ӧ�У� �ǻ�ԭ��������Ӧ����1.5mol���������뷴Ӧ������ת�Ƶĵ��ӵ����ʵ���Ϊ mol���������������� mol��
��4����ҵ������ˮú������H2����ȡ��������������������H2O�е���ԭ�Ӷ�ȫ��ת��ΪNH3����3molH2O���Ƶ� molNH3��
��1�������ܽ���ˮ���õ�����Һ��Ϊ��ˮ�����ܽ���ˮʱ��ˮ������Ӧ����һˮ�ϰ���NH3?H2O��������һ�����д��һˮ�ϰ��ĵ��뷽��ʽ
��2����״���£��� 2.24L�İ�������ˮ��� 0.5L��Һ��������Һ�����ʵ���Ũ��Ϊ
��3��������Cl2��Ӧ����Ӧ����ʽ���£�8NH3+3Cl2�T6NH4Cl+N2�����ø÷�Ӧ��ԭ�����ڹ�ҵ�Ͽ����ڼ������������Ĺܵ��Ƿ�©�����÷�Ӧ�У�
��4����ҵ������ˮú������H2����ȡ��������������������H2O�е���ԭ�Ӷ�ȫ��ת��ΪNH3����3molH2O���Ƶ�
��������1��һˮ�ϰ���һԪ������ֵ��룻һˮ�ϰ���ϡ���ᷴӦ���ɣ�NH4��SO4��
��2������c=
���㣻
��3�����ݷ�Ӧ��Ԫ�ػ��ϼ۵ı仯��������������Ԫ�ش�0�۽��͵�-1�ۣ�1molCl2ת��2mol���ӣ�
��4�����ݷ�Ӧ����ʽ����Ԫ���غ���㣮
��2������c=
| n |
| V |
��3�����ݷ�Ӧ��Ԫ�ػ��ϼ۵ı仯��������������Ԫ�ش�0�۽��͵�-1�ۣ�1molCl2ת��2mol���ӣ�
��4�����ݷ�Ӧ����ʽ����Ԫ���غ���㣮
����⣺��1��һˮ�ϰ���һԪ������ֵ��룬����뷽��ʽΪ��NH3?H2O?NH4++OH-��һˮ�ϰ���ϡ���ᷴӦ���ɣ�NH4��SO4��
�ʴ�Ϊ��NH3?H2O?NH4++OH-����NH4��SO4��
��2����״���£��� 2.24L�İ�������ˮ��� 0.5L��Һ����n��NH3��=0.1mol������c=
=
=0.2mol/L��
�ʴ�Ϊ��0.2��
��3��������Cl2��Ӧ����Ӧ����ʽ���£�8NH3+3Cl2�T6NH4Cl+N2����Ӧ��NԪ�ػ��ϼ����ߣ�����Ϊ��ԭ������������Ԫ�صĻ��ϼ۽��ͣ�����Ϊ����������������Ԫ�ش�0�۽��͵�-1�ۣ�1molCl2ת��2mol���ӣ�����1.5mol�������������뷴Ӧ������ת�Ƶĵ��ӵ����ʵ���Ϊ3mol����8molNH3�μӷ�Ӧʱ��2mol��������ת�Ƶ���Ϊ6mol��
����ת��3mol����ʱ���������İ���Ϊ1mol��
�ʴ�Ϊ��NH3��3��1��
��4����ҵ������ˮú������H2����ȡ��������������������H2O�е���ԭ�Ӷ�ȫ��ת��ΪNH3��������Ԫ���غ㣬
3H2O��2NH3
3mol 2mol
����3molH2O���Ƶ�2molNH3��
�ʴ�Ϊ��2��
�ʴ�Ϊ��NH3?H2O?NH4++OH-����NH4��SO4��
��2����״���£��� 2.24L�İ�������ˮ��� 0.5L��Һ����n��NH3��=0.1mol������c=
| n |
| V |
| 0.1mol |
| 0.5L |
�ʴ�Ϊ��0.2��
��3��������Cl2��Ӧ����Ӧ����ʽ���£�8NH3+3Cl2�T6NH4Cl+N2����Ӧ��NԪ�ػ��ϼ����ߣ�����Ϊ��ԭ������������Ԫ�صĻ��ϼ۽��ͣ�����Ϊ����������������Ԫ�ش�0�۽��͵�-1�ۣ�1molCl2ת��2mol���ӣ�����1.5mol�������������뷴Ӧ������ת�Ƶĵ��ӵ����ʵ���Ϊ3mol����8molNH3�μӷ�Ӧʱ��2mol��������ת�Ƶ���Ϊ6mol��
����ת��3mol����ʱ���������İ���Ϊ1mol��
�ʴ�Ϊ��NH3��3��1��
��4����ҵ������ˮú������H2����ȡ��������������������H2O�е���ԭ�Ӷ�ȫ��ת��ΪNH3��������Ԫ���غ㣬
3H2O��2NH3
3mol 2mol
����3molH2O���Ƶ�2molNH3��
�ʴ�Ϊ��2��
���������⿼����������ʵĵ��뷽��ʽ����д�����ʵ���Ũ�ȼ��㣬������ԭ��Ӧ�е��ӵ�ת��ԭ���غ��Ӧ�õȣ��漰��֪ʶ��϶࣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
 �����ǵ�ѭ���е���Ҫ���ʣ�����������������������Ź㷺��Ӧ�ã�������ѧ֪ʶ���ݴ��������Ҫ��
�����ǵ�ѭ���е���Ҫ���ʣ�����������������������Ź㷺��Ӧ�ã�������ѧ֪ʶ���ݴ��������Ҫ��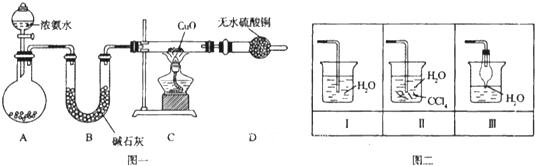

 ________________��
________________��