题目内容
(13分)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_____________________________________________。
(2)若溶液M由10 mL 2 mol·L-1NaHA溶液与2 mol·L-1NaOH溶液等体积混合而得,则溶液M的pH________7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_____________________________________________。
已知Ksp(BaA)=1.8×10-10,向该混合溶液中加入10 mL 1 mol·L-1BaCl2溶液,混合后溶液中的Ba2+浓度为__________ mol·L-1。
(3)若溶液M由下列三种情况:①0.01 mol·L-1的H2A溶液;②0.01 mol·L-1的NaHA溶液;③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为________;pH由大到小的顺序为____________。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为____(填“大于”“等于”“小于”或“均有可能”)。
(1)写出酸H2A的电离方程式_____________________________________________。
(2)若溶液M由10 mL 2 mol·L-1NaHA溶液与2 mol·L-1NaOH溶液等体积混合而得,则溶液M的pH________7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_____________________________________________。
已知Ksp(BaA)=1.8×10-10,向该混合溶液中加入10 mL 1 mol·L-1BaCl2溶液,混合后溶液中的Ba2+浓度为__________ mol·L-1。
(3)若溶液M由下列三种情况:①0.01 mol·L-1的H2A溶液;②0.01 mol·L-1的NaHA溶液;③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为________;pH由大到小的顺序为____________。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为____(填“大于”“等于”“小于”或“均有可能”)。
(1)H2A? H++HA-,HA-?
H++HA-,HA-? ?H++A2-
?H++A2-
(2) > c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) 5.4×10-10
(3)③ ②>③>①
(4)均有可能
 H++HA-,HA-?
H++HA-,HA-? ?H++A2-
?H++A2-(2) > c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) 5.4×10-10
(3)③ ②>③>①
(4)均有可能
⑴水溶液M中存在的离子A2-、HA-说明H2A是弱电解质,是二元弱酸分步电离,H2A的电离方程式H2A?
 H++HA-,HA-?
H++HA-,HA-? ?H++A2-;⑵反应后溶液为Na2A的溶液,A2―水解后呈碱性,pH大于7,HA―水解也生成OH―,所以OH―浓度大于HA―,溶液中离子浓度由大到小顺序为: c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+); 溶液M与BaCl2溶液混合后A2―的浓度为:(10 mL× 2 mol·L-1―10 mL ×1 mol·L-1)/30mL=1/3mol/L,Ksp(BaA)=1.8×10-10=1/3×c(A2-),c(A2-)= 5.4×10-10mol/L;⑶H2A浓度①中为0.01 mol·L-1,②中NaHA水解产生,小于0.01 mol·L-1③相当于0.01 mol·L-1的H2A和NaHA等浓度混合,HA―抑制H2A电离,H2A大于0.01 mol·L-1,③中H2A浓度最大;pH由大到小的顺序为②>③>①;⑷混合后溶液为酸性,但 H2A是强酸还是弱酸末定,NaHA水解和电离相对强弱均不知, V1比V2可能小于、等于、大于都可能。
?H++A2-;⑵反应后溶液为Na2A的溶液,A2―水解后呈碱性,pH大于7,HA―水解也生成OH―,所以OH―浓度大于HA―,溶液中离子浓度由大到小顺序为: c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+); 溶液M与BaCl2溶液混合后A2―的浓度为:(10 mL× 2 mol·L-1―10 mL ×1 mol·L-1)/30mL=1/3mol/L,Ksp(BaA)=1.8×10-10=1/3×c(A2-),c(A2-)= 5.4×10-10mol/L;⑶H2A浓度①中为0.01 mol·L-1,②中NaHA水解产生,小于0.01 mol·L-1③相当于0.01 mol·L-1的H2A和NaHA等浓度混合,HA―抑制H2A电离,H2A大于0.01 mol·L-1,③中H2A浓度最大;pH由大到小的顺序为②>③>①;⑷混合后溶液为酸性,但 H2A是强酸还是弱酸末定,NaHA水解和电离相对强弱均不知, V1比V2可能小于、等于、大于都可能。
练习册系列答案
相关题目
 H++HA-, HA-
H++HA-, HA-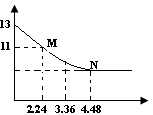
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O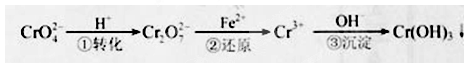
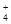 、SO
、SO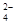 、Cl-
、Cl-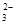
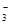 、SCN-
、SCN-