题目内容
(1)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(CH3COO-) c(Na+).(填大于、小于、等于)
(2)将pH=3的硫酸溶液和pH=12的氢氧化钠溶液混和,若使混和后溶液的pH=7,则硫酸溶液和氢氧化钠溶液的体积比是
(3)某酸性化工废水中含有浓度约为0.01mol.L-1的Ag+、Pb2+等重金属离子.有关数据如下:
(i)在废水排放前,用沉淀法除去这两种离子,最好加入 (填字母序号)
A.Na2S、B.NaOH、C.KI、D.Ca(OH)2
(ii)某工程师用CaO处理上述废水后Pb2+的浓度为1.2×10-3 则此溶液的pH= .
(2)将pH=3的硫酸溶液和pH=12的氢氧化钠溶液混和,若使混和后溶液的pH=7,则硫酸溶液和氢氧化钠溶液的体积比是
(3)某酸性化工废水中含有浓度约为0.01mol.L-1的Ag+、Pb2+等重金属离子.有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-12 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.Na2S、B.NaOH、C.KI、D.Ca(OH)2
(ii)某工程师用CaO处理上述废水后Pb2+的浓度为1.2×10-3 则此溶液的pH=
分析:(1)pH=3的醋酸,c(醋酸)>0.001mol/L,pH=11的氢氧化钠,c(NaOH)=0.001mol/L,等体积混合,醋酸过量,电荷守恒为c(CH3COO-)+c(OH-)=c(Na+)+c(H+);
(2)混和后溶液的pH=7,则酸中n(H+)=碱中n(OH-);
(3)(i)用沉淀法除去这两种离子,由表格中溶度积数据可知,硫化物的溶度积小,易转化为沉淀;
(ii)用CaO处理上述废水后Pb2+的浓度为1.2×10-3,利用Pb(OH)2的Ksp计算.
(2)混和后溶液的pH=7,则酸中n(H+)=碱中n(OH-);
(3)(i)用沉淀法除去这两种离子,由表格中溶度积数据可知,硫化物的溶度积小,易转化为沉淀;
(ii)用CaO处理上述废水后Pb2+的浓度为1.2×10-3,利用Pb(OH)2的Ksp计算.
解答:解:(1)pH=3的醋酸,c(醋酸)>0.001mol/L,pH=11的氢氧化钠,c(NaOH)=0.001mol/L,等体积混合,醋酸过量,溶液呈酸性,c(OH-)<c(H+),由电荷守恒为c(CH3COO-)+c(OH-)=c(Na+)+c(H+),则c(CH3COO-)>c(Na+),
故答案为:酸性;大于;
(2)混和后溶液的pH=7,则酸中n(H+)=碱中n(OH-),则V酸×10-3=V碱×10-2,硫酸溶液和氢氧化钠溶液的体积比是10:1,故答案为:10:1;
(3)(i)用沉淀法除去这两种离子,由表格中溶度积数据可知,硫化物的溶度积小,易转化为沉淀,则最后选择硫化钠,故答案为:A;
(ii)用CaO处理上述废水后Pb2+的浓度为1.2×10-3,由Pb(OH)2的Ksp可知,c(OH-)=
=10-6mol/L,则c(H+)=10-8mol/L,所以pH=8,
故答案为:8.
故答案为:酸性;大于;
(2)混和后溶液的pH=7,则酸中n(H+)=碱中n(OH-),则V酸×10-3=V碱×10-2,硫酸溶液和氢氧化钠溶液的体积比是10:1,故答案为:10:1;
(3)(i)用沉淀法除去这两种离子,由表格中溶度积数据可知,硫化物的溶度积小,易转化为沉淀,则最后选择硫化钠,故答案为:A;
(ii)用CaO处理上述废水后Pb2+的浓度为1.2×10-3,由Pb(OH)2的Ksp可知,c(OH-)=
|
故答案为:8.
点评:本题考查较综合,涉及pH的计算,酸碱混合的计算、溶度积的计算等,为高考高频考点,侧重学生分析问题解决问题能力及计算能力的考查,题目难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
已知反应:
①101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1
下列结论正确的是( )
①101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1
下列结论正确的是( )
| A、碳的燃烧热等于110.5 kJ?mol-1 | B、2mol C(s)在1mol O2(g)燃烧,放出221 kJ热量 | C、1L0.1mol/L H2SO4溶液与1L0.1mol/L NaOH溶液反应,放出5.73kJ热量 | D、pH=3的醋酸与pH=11的NaOH溶液反应生成1mol水,放出57.3kJ热量 |
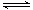 2HI的平衡体系,加压后密闭体系中的混合气体密度增加
2HI的平衡体系,加压后密闭体系中的混合气体密度增加