��Ŀ����
����Ŀ��ij̽���С��������ԭ��ط�Ӧ�������Ļ��˳���мס�����λͬѧ��ʹ��þƬ����Ƭ���缫������ͬѧ���缫����6 mol��L��1��ϡH2SO4�У���ͬѧ���缫����6 mol��L��1��NaOH��Һ�У���ͼ��ʾ��
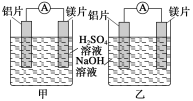
(1)д���׳��з������йص缫��Ӧ�ķ�Ӧʽ��
����___________________________________��
����___________________________________��
(2)д���ҳ��з������йص缫��Ӧ�ķ�Ӧʽ��
����___________________________________��
����___________________________________��
�ܷ�Ӧ���ӷ���ʽΪ_________________________��
(3)�����������λͬѧ����Ϊ������ԭ��صĵ缫�������ǽ������ɸ������ϵĽ���Ӧ�ȹ����������ϵĽ������á�������жϳ�________��Ը�ǿ�����һ��жϳ�________��Ը�ǿ(��дԪ�ط���)��
(4)�ɴ�ʵ�飬�ɵõ�������Щ���ۣ�________��
A������ԭ��ط�Ӧ�жϽ������˳��Ӧע��ѡ����ʵĽ���
B��þ�Ľ����Բ�һ�������Ľ�����ǿ
C����ʵ��˵���������˳����ѹ�ʱ����û��ʵ�ü�ֵ
D����ʵ��˵����ѧ�о������ӡ���Ӧ������䣬Ӧ��������������
(5)����ʵ��Ҳ������֤���ˡ����ý������˳���ֱ���ж�ԭ���������������������________(��ɿ������ɿ���)���粻�ɿ��������������һ���ж�ԭ��������������е�ʵ�鷽��____________________��
���𰸡�(1)Mg��2e��===Mg2�� 2H����2e��===H2��
(2)2Al��8OH����6e��===2AlO2����4H2O
6H2O��6e��===6OH����3H2��
2Al��2OH����2H2O===2AlO2����3H2��
(3)Mg Al (4)AD
(5)���ɿ� �����ֽ����缫���ϵ�����������ԭ��أ����õ������������ķ��Ӷ��жϵ��ӵ�������������ȷ��ԭ��ص���������
��������(1)�׳��е���ܷ�Ӧ����ʽΪMg��H2SO4===MgSO4��H2����Mg���������缫��ӦʽΪMg��2e��===Mg2����Al���������缫��ӦʽΪ2H����2e��===H2����
(2)�ҳ��е���ܷ�Ӧ����ʽΪ2Al��2NaOH��2H2O===2NaAlO2��3H2����������ΪAl����������Al3������OH����Ӧ����AlO2�����缫��ӦʽΪ2Al��6e����8OH��===2AlO2����4H2O����������ΪH2���缫��ӦʽΪ6H2O��6e��===6OH����3H2����
(3)�׳���MgΪ������AlΪ�������ҳ���AlΪ������MgΪ�����������ݸ������Ͻ������������ã�����ж�Mg���ǿ�����ж�Al���ǿ��
(4)ѡAD��Mg�Ľ������һ����Alǿ���������˳�������ȷ�ģ�Ӧ�ù㷺��
(5)�ж����������ɸ��ݻ�·�е���������������Ƚ����жϣ�ֱ�����ý������˳����ж�ԭ��ص����������Dz��ɿ��ġ�


