题目内容
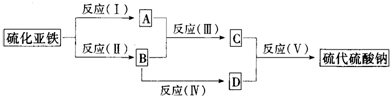
 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图所示(部分反应中的水已略去).(1)若A为强碱,其焰色反应显黄色,C为厨房中用品.
①D的化学式是
CO2
CO2
.②反应Ⅲ的离子方程式是
HCO3-+OH-=H2O+CO32-
HCO3-+OH-=H2O+CO32-
.(2)若A、D均为单质,且A为黄绿色气体,D元素的一种红棕色氧化物常用作颜料.
①反应Ⅲ的离子方程式是
Cl2+2Fe2+=2Cl-+2Fe3+
Cl2+2Fe2+=2Cl-+2Fe3+
.②B与明矾均可作净水剂,B可以净水的原理是
Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
 Fe(OH)3+3H+
Fe(OH)3+3H+Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
. Fe(OH)3+3H+
Fe(OH)3+3H+(3)将NaI溶液与(1)中A和(2)中的A混合可以制得一种化工原料,若消耗0.1mol NaI转移电子0.6mol,则三种物质间发生化学反应的离子方程式是
3Cl2+6OH-+I-=6Cl-+IO3-+3H2O
3Cl2+6OH-+I-=6Cl-+IO3-+3H2O
.分析:(1)若A为强碱,其焰色反应显黄色,应为NaOH,C为厨房中用品,结合转化关系可知B为Na2CO3,C为NaHCO3,D为CO2;
(2)若A、D均为单质,且A为黄绿色气体,应为Cl2,D元素的一种红棕色氧化物常用作颜料,则D为Fe,B为FeCl3,C为FeCl2;
(3)若消耗0.1mol NaI转移电子0.6mol,则I的化合价由-1价升高到+5价,应与NaOH和Cl2反应生成NaIO3.
(2)若A、D均为单质,且A为黄绿色气体,应为Cl2,D元素的一种红棕色氧化物常用作颜料,则D为Fe,B为FeCl3,C为FeCl2;
(3)若消耗0.1mol NaI转移电子0.6mol,则I的化合价由-1价升高到+5价,应与NaOH和Cl2反应生成NaIO3.
解答:解:(1)若A为强碱,其焰色反应显黄色,应为NaOH,C为厨房中用品,结合转化关系可知B为Na2CO3,
C为NaHCO3,D为CO2,
①由以上分析可知D为CO2,故答案为:CO2;
②反应Ⅲ为NaHCO3和NaOH的反应,反应的离子方程式是HCO3-+OH-=H2O+CO32-,
故答案为:HCO3-+OH-=H2O+CO32-;
(2)若A、D均为单质,且A为黄绿色气体,应为Cl2,D元素的一种红棕色氧化物常用作颜料,则D为Fe,
B为FeCl3,C为FeCl2,
①反应Ⅲ为FeCl2和Cl2的反应,反应的离子方程式是Cl2+2Fe2+=2Cl-+2Fe3+,
故答案为:Cl2+2Fe2+=2Cl-+2Fe3+;
②FeCl3可以净水,原因是Fe3+水解生成具有吸附性的Fe(OH)3,
反应的离子方程式为Fe3++3H2O Fe(OH)3+3H+,
Fe(OH)3+3H+,
故答案为:Fe3++3H2O Fe(OH)3+3H+;
Fe(OH)3+3H+;
(3)若消耗0.1mol NaI转移电子0.6mol,则I的化合价由-1价升高到+5价,应与NaOH和Cl2反应生成NaIO3,反应的离子方程式为3Cl2+6OH-+I-=6Cl-+IO3-+3H2O,
故答案为:3Cl2+6OH-+I-=6Cl-+IO3-+3H2O.
C为NaHCO3,D为CO2,
①由以上分析可知D为CO2,故答案为:CO2;
②反应Ⅲ为NaHCO3和NaOH的反应,反应的离子方程式是HCO3-+OH-=H2O+CO32-,
故答案为:HCO3-+OH-=H2O+CO32-;
(2)若A、D均为单质,且A为黄绿色气体,应为Cl2,D元素的一种红棕色氧化物常用作颜料,则D为Fe,
B为FeCl3,C为FeCl2,
①反应Ⅲ为FeCl2和Cl2的反应,反应的离子方程式是Cl2+2Fe2+=2Cl-+2Fe3+,
故答案为:Cl2+2Fe2+=2Cl-+2Fe3+;
②FeCl3可以净水,原因是Fe3+水解生成具有吸附性的Fe(OH)3,
反应的离子方程式为Fe3++3H2O
 Fe(OH)3+3H+,
Fe(OH)3+3H+,故答案为:Fe3++3H2O
 Fe(OH)3+3H+;
Fe(OH)3+3H+;(3)若消耗0.1mol NaI转移电子0.6mol,则I的化合价由-1价升高到+5价,应与NaOH和Cl2反应生成NaIO3,反应的离子方程式为3Cl2+6OH-+I-=6Cl-+IO3-+3H2O,
故答案为:3Cl2+6OH-+I-=6Cl-+IO3-+3H2O.
点评:本题考查较为综合,涉及元素化合物的推断和应用,侧重于考查学生元素化合物知识的综合运用能量,注意掌握相关化学知识,难度中等.

练习册系列答案
相关题目