题目内容
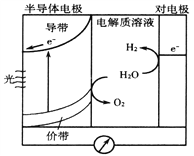
【题目】(1)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图1所示装置中,以稀土金属材料作惰性电极,在电极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。
已知:正极反应式:O2-4e-=2O2-。

则:c电极的名称为__,d电极上的电极反应式为__。
(2)如图2所示,用惰性电极电解100mL0.5molL-1CuSO4溶液,a电极上的电极反应式为__,若a电极产生56mL(标准状况)气体,则所得溶液的pH=_(不考虑溶液体积变化)。
【答案】正极 CH4+4O2--8e-=CO2+2H2O 4OH--4e-=2H2O+O2↑或2H2O-4e-=4H++O2↑ 1
【解析】
(1)依据装置图中电流流向分析,c为正极,氧气得电子发生还原反应,d为负极,甲烷失电子发生氧化反应;
(2)图乙是电解池,与电源正极连接的a电极为阳极,电极反应为4OH--4e-=O2↑+2H2O,b为阴极,电极反应为Cu2++2e-=Cu,结合电极方程式计算。
(1)图甲是原电池,依据电流流向是从正极流向负极,c电极为正极,氧气得到电子发生还原反应,d电极为电池负极,甲烷失电子发生氧化反应,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子,负极电极反应为:CH4-8e-+4O2-=CO2+2H2O;
(2)如图乙所示电解100mL0.5molL-1CuSO4溶液,发生的电解总反应为:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,与电源正极相连的a极为阳极,溶液中氢氧根离子失去电子发生氧化反应,电极反应为:2H2O-4e-=4H++O2↑或者4OH--4e-=2H2O+O2↑;若a电极产生56mL(标准状况)氧气,氧气物质的量为0.0025mol,溶液中生成氢离子物质的量为0.01mol,c(H+)=
2Cu+O2↑+2H2SO4,与电源正极相连的a极为阳极,溶液中氢氧根离子失去电子发生氧化反应,电极反应为:2H2O-4e-=4H++O2↑或者4OH--4e-=2H2O+O2↑;若a电极产生56mL(标准状况)氧气,氧气物质的量为0.0025mol,溶液中生成氢离子物质的量为0.01mol,c(H+)=![]() =0.1mol/L,pH=-lg0.1=1。
=0.1mol/L,pH=-lg0.1=1。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案