题目内容
在由Fe、FeO、和Fe2O3组成的混合物中加入100 mL2 mol ·L—1的盐酸,恰好使混合物完全溶解,并放出448mL气体(标准状况),此时溶液中无Fe3+离子,则下列判断正确的是
| A.混合物里3种物质反应时消耗盐酸的物质的量浓度之比为1︰1︰3 |
| B.反应后所得溶液中的Fe2+离子与Cl-离子的物质的量浓度之比为2︰1 |
| C.混合物里,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多 |
| D.混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
C
解析试题分析:n(Cl-)=0.2mol,反应后的溶液为FeCl2.溶液,n(Fe2+)=0.1mol.所以n(Fe2+):n(Cl-)=1:2可能发生的反应(1)Fe2O3+6HCl=2FeCl3+3H2O; (2)FeO+2HCl=FeCl2+H2O; (3)Fe+2FeCl3=3FeCl2.;(4)Fe+2HCl=FeCl2+H2↑.发生反应产生氢气的铁的物质的量为n(Fe)=0.448L÷22.4mol/L=0.02mol.铁还发生(3)的反应。由(1)(3)可得关系式Fe--2FeCl3--Fe2O3,所以铁的物质的量比Fe2O3的物质的量多。但无法确定氧化亚铁的物质的量的多少。选项为:C。
考点:考查Fe、FeO、和Fe2O3组成的混合物与盐酸反应的知识。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案下列各组物质相互反应后,再向得到的溶液中滴入KSCN试剂,溶液变成红色的是
| A.氯水和氯化亚铁溶液 | B.铁屑和氯化铜溶液 |
| C.铁屑和过量稀硫酸 | D.过量铁屑和氯化铁溶液 |
1 L某混合溶液中,溶质X、Y浓度都为0.1mol·L—1,向混合溶液中滴加0.1 mol·L—1某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是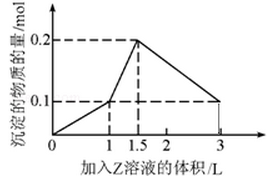
| A.氯化铝、氯化镁、氢氧化钠 |
| B.偏铝酸钠、氢氧化钡、硫酸 |
| C.氯化铝、氯化铁、氢氧化钠 |
| D.偏铝酸钠、氯化钡、硫酸 |
将含1 mol Na和1 mol Al的合金加入足量的水中,下列描述不正确的是 ( )
| A.金属Al无剩余 | B.c(Na+)=c(AlO-2) |
| C.生成气体为2 mol | D.c(Na+)=c(Al3+) |
有两瓶失去标签的物质的量浓度相同的Na2CO3和NaHCO3稀溶液。下列鉴别方法和所得到的结论不正确的是 ( )
| A.取少量未知溶液两份,分别滴加Ba(NO3)2溶液,有沉淀生成的为Na2CO3溶液 |
| B.取少量未知溶液两份,分别滴加几滴酚酞试液,红色较深的是NaHCO3溶液 |
| C.取少量未知溶液两份,分别滴加稀盐酸溶液,立即有气泡产生的是NaHCO3溶液 |
| D.用pH试纸测定两溶液的pH,pH较小的为Na2CO3溶液 |
在FeCl3和CuCl2混合液中,加入一定量的铁粉,充分反应后,溶液中的金属离子不可能是
| A.有Fe2+ | B.Cu2+、Fe2+ 和Fe3+ |
| C.仅有 Fe3+ 和Fe2+ | D.有Cu2+和Fe2+ |
1L某混合溶液中,溶质X、Y的浓度都为0.1mol?L﹣1,向混合溶液中滴加某溶液Z(0.1mol?L﹣1氢氧化钠或硫酸溶液)至溶液呈中性,所得沉淀的物质的量如图所示,则X、Y、Z分别是( )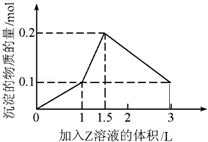
| A.氯化铝、氯化铁、氢氧化钠 | B.氯化铝、氯化镁、氢氧化钠 |
| C.偏铝酸钠、氢氧化钡、硫酸 | D.偏铝酸钠、氯化钡、硫酸 |
把生锈的铁钉放入足量稀盐酸中,可能发生的反应是( )
| A.只有置换反应 | B.只有复分解反应 |
| C.置换和复分解反应 | D.置换和分解反应 |
常温常压下,将amolCO2气体通入1Lbmol/L的NaOH溶液中,下列对所得溶液的描述不正确的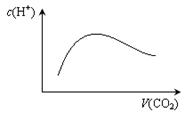
| A.当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如右图变化关系 |
| B.当a=b时,所得溶液中存在:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| C.当2a=b时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| D.当1/2<a/b<1时,所得溶液中一定存在:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |