题目内容
(2011?烟台模拟)【化学-物质结构与性质】
含氯化合物在自然界中广泛存在.
(1)CuCl是一种白色粉末,常用作有机机合成催化剂、颜料.试写出基态Cu+离子的核外电子排布式
(2)碳、氧、氯三种元素形成一种化合物,俗称光气.其分子中含有四个原子,每个原子的最外层都达到8电子的稳定结构,则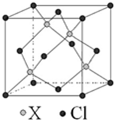 碳原子的杂化轨道类型为
碳原子的杂化轨道类型为
(3)氯化铝在177.8℃时升华,蒸气或熔融状态以Al2Cl6形式存在.下列关于氯化铝的推断错误的是
a.氯化铝为共价化合物 b.Al2Cl6中存在配位键 c.氯化铝难溶于有机溶剂
(4)某金属元素X与氯元素形成的晶体结构如图所示,则该晶体的化学式为
含氯化合物在自然界中广泛存在.
(1)CuCl是一种白色粉末,常用作有机机合成催化剂、颜料.试写出基态Cu+离子的核外电子排布式
1s22s22p63s23p63d10
1s22s22p63s23p63d10
.(2)碳、氧、氯三种元素形成一种化合物,俗称光气.其分子中含有四个原子,每个原子的最外层都达到8电子的稳定结构,则
 碳原子的杂化轨道类型为
碳原子的杂化轨道类型为sp2
sp2
,该分子中含有3
3
个σ键.(3)氯化铝在177.8℃时升华,蒸气或熔融状态以Al2Cl6形式存在.下列关于氯化铝的推断错误的是
C
C
.a.氯化铝为共价化合物 b.Al2Cl6中存在配位键 c.氯化铝难溶于有机溶剂
(4)某金属元素X与氯元素形成的晶体结构如图所示,则该晶体的化学式为
XCl
XCl
.分析:(1)铜是29号元素,铜原子失去一个电子变成亚铜离子,则亚铜离子核外有28个电子,根据 构造原理写出亚铜离子核外电子排布式;
(2)根据光气分子中碳原子含有的价层电子对确定其杂化方式,根据其结构式确定含有的 σ键个数;
(3)根据氯化铝的熔点确定其晶体类型,熔点较低的化合物一般为分子晶体,氯化铝易溶于有机溶剂;
(4)利用均摊法确定其化学式.
(2)根据光气分子中碳原子含有的价层电子对确定其杂化方式,根据其结构式确定含有的 σ键个数;
(3)根据氯化铝的熔点确定其晶体类型,熔点较低的化合物一般为分子晶体,氯化铝易溶于有机溶剂;
(4)利用均摊法确定其化学式.
解答:解:(1)铜原子失去一个电子变成亚铜离子,失电子时先失去最外层电子,所以其核外电子排布式为:1s22s22p63s23p63d10,故答案为:1s22s22p63s23p63d10;
(2)光气的结构式为 ,碳原子含有3个σ键,且不含孤电子对,所以采取sp2杂化,故答案为:sp2;3;
,碳原子含有3个σ键,且不含孤电子对,所以采取sp2杂化,故答案为:sp2;3;
(3)氯化铝熔点较低,所以为分子晶体,分子中只含共价键,所以为共价化合物,蒸气或熔融状态以Al2Cl6形式存在,氯化铝中铝原子最外层电子只有3个电子,每个铝原子和四个氯原子形成共价键,且其中一个共用电子对是氯原子提供,所以含有配位键,氯化铝易溶于水和有机溶剂,故选c;
(4)该晶胞中,X离子个数=4,氯离子个数=8×
+6×
=4,X和氯离子个数比=4:4=1:1,所以其化学式为XCl,故答案为:XCl.
(2)光气的结构式为
 ,碳原子含有3个σ键,且不含孤电子对,所以采取sp2杂化,故答案为:sp2;3;
,碳原子含有3个σ键,且不含孤电子对,所以采取sp2杂化,故答案为:sp2;3;(3)氯化铝熔点较低,所以为分子晶体,分子中只含共价键,所以为共价化合物,蒸气或熔融状态以Al2Cl6形式存在,氯化铝中铝原子最外层电子只有3个电子,每个铝原子和四个氯原子形成共价键,且其中一个共用电子对是氯原子提供,所以含有配位键,氯化铝易溶于水和有机溶剂,故选c;
(4)该晶胞中,X离子个数=4,氯离子个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
点评:本题考查物质结构,涉及化学式的确定、杂化方式的确定、核外电子排布式的书写等知识,利用均摊法、价层电子对互斥理论、构造原理来分析解答即可,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2011?烟台模拟)水的电离平衡曲线如图所示:
(2011?烟台模拟)水的电离平衡曲线如图所示: