题目内容
【题目】【2014新课标2】37.[化学选修——3:物质结构与性质]
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图为 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥结构的酸是 。(填化学式)
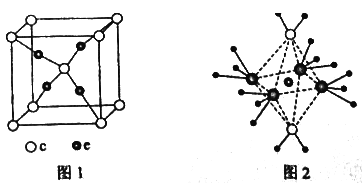
(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 。
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是 ,判断理由是 。
【答案】
(1)N ![]()
(2)sp3 H2O2、N2H4
(3)HNO2、HNO3 H2SO3
(4)+1
(5)SO42— 共价键和配位键 H2O H2O与Cu2+的配位键比NH3与Cu2+的弱
【解析】本题的解题要点为:能根据常见元素的原子结构及在元素周期表的位置准确推断相关元素,掌握元素原子核外电子排布规律及元素周期律,掌握化学键的类型与分子结构与分子性质的关系,掌握晶胞的分析方法。根据题意知,周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其电子层数相同,则a为氢元素;b的价电子层中的未成对电子有3个,则b为氮元素;c的最外层电子数为其内层电子数的3倍,则c为氧元素;d与c同主族,则d为硫元素;e的最外层只有1个电子,但次外层有18个电子,则e为铜元素。
(1)同周期由左向右第一电离能呈递增趋势,但当元素原子的轨道呈全满、全空、半充满状态时,较稳定;同主族由上到下第一电离能逐渐减小。氮原子2p轨道为半充满状态,较稳定,则N、O、S中第一电离能最大的是N;e为铜元素,价层电子轨道示意图为![]() 。
。
(2)a为氢元素,和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子为氨分子,中心原子的杂化方式为sp3;分子中既含有极性共价键,又含有非极性共价键的化合物是H2O2、N2H4、C2H6等。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是HNO2、HNO3;酸根呈三角锥结构的酸是H2SO3。
(4)根据O和Cu形成的离子化合物的晶胞结构判断,该化合物的化学式为Cu2O,则e离子的电荷为+1。
(5)根据题给信息知,这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,为硫酸根;阳离子呈轴向狭长的八面体结构结合图2知,该化合物的化学式为[Cu(NH3)4(H2O)2]SO4。则该化合物中阴离子为SO42—,阳离子中存在的化学键类型有共价键和配位键;该化合物加热时首先失去的组分是H2O,判断理由是H2O与Cu2+的配位键比NH3与Cu2+的弱。

【题目】苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:


名称 | 性状 | 熔点/℃ | 沸点/℃ | 密度(g/mL) | 水溶性 |
甲苯 | 无色易挥发液体 | -95 | 110.6 | 0.8669 | 不溶 |
苯甲酸 | 白色晶体 | 112.4 | 248 | 1.2659 | 微溶 |
苯甲酸在水中的溶解度表:
温度/℃ | 25 | 50 | 95 |
溶解度/g | 0.344 | 0.849 | 6.8 |
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈瓶中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g KMnO4(过量),继续搅拌约4~5 h,直至反应完全,停止加热和搅拌,静置。
二、分离提纯
将反应混合液放在冰水浴中冷却,然后用稀硫酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,干燥,得到粗产品。
三、测定纯度
称取m g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3指示剂,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)仪器a的名称是____________,其作用为_________________________。
(3)分离提纯阶段产品减压过滤时用冷水洗涤的原因是______________________________。
(4)进一步提纯苯甲酸粗产品的操作是_____________。
(5)测定纯度阶段,所选的指示剂为_________,滴定终点的现象是________________。若m=1.200 g,滴定时用去0.1200 mol/L标准KOH溶液20.00 mL,则所得产品中苯甲酸的纯度(质量分数)为_________。
【题目】实验室用环己醇脱水的方法合成环己烯,该实验的装置如下图所示:

可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是________;b的名称是________;
(2)a中发生主要反应的化学方程式为____________________________;本实验最容易产生的有机副产物的结构简式为________。
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加人无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是________,操作X的名称为________。
Ⅲ.产物分析及产率计算
(4)①核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有_______种不同化学环境的氢原子。
② 本实验所得环己烯的产率是_______。

