题目内容
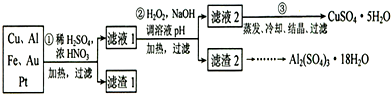
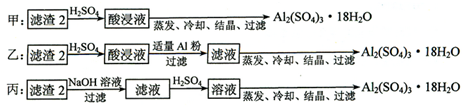
硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一.如图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:

(1)要将上流程图中洗出液中的溶质析出,采用的方法是______.
A.蒸发结晶 B.冷却结晶
C.先蒸发,再冷却结晶 D.先冷却,再蒸发结晶
(2)在以上流程中,要将洗净的石英砂研磨成粉末,目的是______.
A.增加反应物的浓度,增大化学反应速率,提高生产效率.
B.作为催化剂载体,增加反应物与催化剂接触面积,增加反应速率,提高生产效率.
C.增加反应物之间的接触面积,增大反应速率,提高生产效率.
D.增加正反应速率,减小逆反应速率,使平衡向正反应方向移动,降低生产成本.
(3)蒸发时用到的硅酸盐仪器有______.
(4)上流程中加入NaOH溶液,反应的离子方程式是______.
(5)硅酸钠溶液呈碱性,其原因是(用一离子方程式表示)______.硅酸钠的用途很广,其中的一种用途是______.
(6)用上流程中的残渣来焊接铁轨,反应的化学方程式是______.
解:(1)石英砂(含氯化钠、氧化铁等杂质)水洗涤得到洗出液,中主要是氯化钠溶液,氯化钠溶解度随温度变化不大,可以利用蒸发结晶的方法得到溶质;冷却结晶适用于溶解度随温度变化大的物质,BCD不符合,故答案为:A.
(2)要将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;
A、固体物质无难度变化,故A错误;
B、不是催化剂的载体,故B错误;
C、增加反应物之间的接触面积,增大反应速率,提高生产效率,故C正确;
D、正逆反应速率都增大,但不影响平衡,故D错误;
故选C.
(3)蒸发时用到的硅酸盐仪器是玻璃仪器和陶瓷仪器有蒸发皿,酒精灯,玻璃棒;
故答案为:蒸发皿,酒精灯,玻璃棒;
(4)上流程中加入NaOH溶液是为了溶解二氧化硅除去杂质,反应的离子方程式:SO2+2OH-=SO32-+H2O;
故答案为:SO2+2OH-=SO32-+H2O;
(5)硅酸钠溶液呈碱性是因为硅酸根离子水解生成硅酸和氢氧根离子,反应的离子方程式为:SiO32-+2H2O?H2SiO3+2OH-;硅酸钠的用途很广,其中的一种用途是,黏合剂或防腐剂或合成洗涤剂或制备硅胶或分子筛;
故答案为:SiO32-+2H2O?H2SiO3+2OH-;黏合剂或防腐剂或合成洗涤剂或制备硅胶或分子筛;
(6)流程中的残渣是Fe2O3来焊接铁轨的反应原理是利用铝热反应,反应的化学方程式 为:2Al+Fe2O3 2Fe+Al2O3;
2Fe+Al2O3;
故答案为:2Al+Fe2O3 2Fe+Al2O3 ;
2Fe+Al2O3 ;
分析:(1)石英砂(含氯化钠、氧化铁等杂质)水洗涤得到洗出液,中主要是氯化钠溶液,氯化钠溶解度随温度变化不大,可以利用蒸发结晶的方法得到溶质;
(2)将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;
(3)蒸发时用到的硅酸盐仪器是玻璃、陶瓷仪器,主要有蒸发皿,玻璃棒、酒精灯;
(4)加入氢氧化钠溶液是为了溶解二氧化硅除去;
(5)硅酸钠溶液呈碱性是因为硅酸根水解生成硅酸和氢氧根离子;依据硅酸钠的性质回答用途;
(6)流程中的残渣分析判断为氧化铁,利用铝热反应进行焊接钢轨
点评:本题考查了物质制备的流程分析和过程反应,盐类水解的应用,实验仪器的选择和组成分析,化学反应速率的影响因素,题目难度中等.
(2)要将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;
A、固体物质无难度变化,故A错误;
B、不是催化剂的载体,故B错误;
C、增加反应物之间的接触面积,增大反应速率,提高生产效率,故C正确;
D、正逆反应速率都增大,但不影响平衡,故D错误;
故选C.
(3)蒸发时用到的硅酸盐仪器是玻璃仪器和陶瓷仪器有蒸发皿,酒精灯,玻璃棒;
故答案为:蒸发皿,酒精灯,玻璃棒;
(4)上流程中加入NaOH溶液是为了溶解二氧化硅除去杂质,反应的离子方程式:SO2+2OH-=SO32-+H2O;
故答案为:SO2+2OH-=SO32-+H2O;
(5)硅酸钠溶液呈碱性是因为硅酸根离子水解生成硅酸和氢氧根离子,反应的离子方程式为:SiO32-+2H2O?H2SiO3+2OH-;硅酸钠的用途很广,其中的一种用途是,黏合剂或防腐剂或合成洗涤剂或制备硅胶或分子筛;
故答案为:SiO32-+2H2O?H2SiO3+2OH-;黏合剂或防腐剂或合成洗涤剂或制备硅胶或分子筛;
(6)流程中的残渣是Fe2O3来焊接铁轨的反应原理是利用铝热反应,反应的化学方程式 为:2Al+Fe2O3
 2Fe+Al2O3;
2Fe+Al2O3;故答案为:2Al+Fe2O3
 2Fe+Al2O3 ;
2Fe+Al2O3 ;分析:(1)石英砂(含氯化钠、氧化铁等杂质)水洗涤得到洗出液,中主要是氯化钠溶液,氯化钠溶解度随温度变化不大,可以利用蒸发结晶的方法得到溶质;
(2)将洗净的石英砂研磨成粉末是增大接触面积,加快反应速率,提高生产效率;
(3)蒸发时用到的硅酸盐仪器是玻璃、陶瓷仪器,主要有蒸发皿,玻璃棒、酒精灯;
(4)加入氢氧化钠溶液是为了溶解二氧化硅除去;
(5)硅酸钠溶液呈碱性是因为硅酸根水解生成硅酸和氢氧根离子;依据硅酸钠的性质回答用途;
(6)流程中的残渣分析判断为氧化铁,利用铝热反应进行焊接钢轨
点评:本题考查了物质制备的流程分析和过程反应,盐类水解的应用,实验仪器的选择和组成分析,化学反应速率的影响因素,题目难度中等.

练习册系列答案
相关题目
下表所列举的各组事实中,存在因果关系的是
| 选项 | 陈述I | 陈述Ⅱ |
| A | SO3可与水反应 | 工业生产硫酸用水吸收SO3 |
| B | Cl2和SO2都有较好的漂白作用 | Cl2和SO2混合后可用于漂白纸浆 |
| C | 铝的最外层电子较钠多 | 钠的金属性强于铝 |
| D | 石墨常用作电解池的电极 | 石墨的化学性质稳定且导电性好 |
- A.A
- B.B
- C.C
- D.D