��Ŀ����
����Ŀ����ѧʵ���У���ʹij���е��к�������Ϊ��һ���ķ�Ӧ��γ�һ��ѭ�����Ϳɲ������ŷŸ����к����ʡ����磺

��l���������б�ŵIJ����У����û�ԭ������_______����������������___________ �����ţ���
������ѭ���У�������ǿ�ᷴӦ������ǿ�Ӧ������������______���ѧʽ����
��3����ɲ���ƽ����ٵĻ�ѧ����ʽ�����õ����ŷ��������ת�Ƶķ������Ŀ��_______��
��Na2Cr2O7����KI����HCl����CrCl3����NaCl����KCl����I2����
���𰸡� �� �� Cr(OH)3 1 6 14 2 2 6 3��7H2O��![]()
��������(1)��Ӧ�Т�CrԪ�ػ��ϼ۽��ͣ���Ҫ�ӻ�ԭ������CrԪ�ػ��ϼ����ߣ���Ҫ�����������ڢ�CrԪ�ػ��ϼ۲��䣬��Ϊ���֮��ķ�Ӧ���ɢ۵ķ�Ӧ���������������ԣ���֪����ѭ���У�������ǿ�ᷴӦ������ǿ�Ӧ������������Cr(OH)3��
(2)CrԪ�ػ��ϼ���+6�۽���Ϊ+3�ۣ�IԪ�صĻ��ϼ���-1������Ϊ0���ɵ��ӡ�ԭ���غ��֪����ӦΪNa2Cr2O7+6KI+14HCl=2CrCl3+2NaCl+6KCl+3I2+7H2O���÷�Ӧת��6e-���õ����ű�ʾ����ת�Ƶķ�����ĿΪ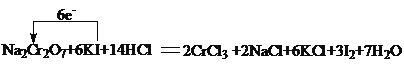 ��
��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���¶�ΪTʱ����2.0L�����ܱ������г���1.0 molPCl5����ӦPCl5(g)![]() PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ����(����)
A. ��Ӧ��ǰ50 s��ƽ������Ϊv(PCl3)=0.0032 mol��L��1��s��1
B. ���������������䣬�����¶ȣ�ƽ��ʱ��c(PCl3)=0.11 mol��L��1,��Ӧ����H��0
C. ��ͬ�¶��£���ʼʱ�������г���1.0molPCl5��0.20molPCl3��0.20molCl2���ﵽƽ��ǰv(��)��v(��)
D. ��ͬ�¶��£���ʼʱ�������г���2.0molPCl3��2.0molCl2���ﵽƽ��ʱ��PCl3��ת����С��80%

