题目内容
(1)只用一种试剂即可除去少量杂质和鉴别物质。将其填在空格处。
编号 | 物质 | 试剂名称或化学式 |
① | 除杂质:NaHCO3溶液(Na2CO3) |
|
② | 除杂质:SiO2(CaCO3) |
|
③ | 除杂质:FeCl2溶液(FeCl3) |
|
④ | 鉴别:Na2CO3 Na2SiO3 Na2SO3 溶液 |
|
⑤ | 鉴别:(NH4)2SO4 NH4C1 Na2SO4溶液 |
|
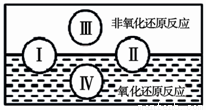
(2)氧化还原是常见的反应类型,根据信息回答以下问题: “四种基本反应类型与氧化还原反应的关系”也可用下图表达。其 中Ⅰ为化合反应,则Ⅱ为 反应。写出一个有水生成的符合反应类型Ⅲ的化学方程式: 。写出一个有水参加的符合反应类型Ⅳ的化学方程式 ,其中水作为 剂。(填氧化剂、还原剂等)
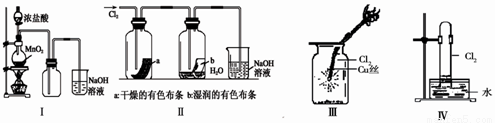
(3)将SO2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,溶液不褪色。经实验证明,SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是 。
(1)①二氧化碳 ②盐酸 ③ 铁屑 ④ 盐酸 ⑤ 氢氧化钡溶液
(2)分解; III方程式合理即可.IV方程式合理即可
与金属反应水为氧化剂。与氟反应水为还原剂。与氯气反应水既不是氧化剂也不是还原剂。
(3)(2分)SO2+C12+2H2O===4H++SO42-+2Cl-
【解析】
试题分析:(1)①Na2CO3与CO2、H2O反应生成NaHCO3,所以加入CO2可除去杂质Na2CO3。
②盐酸与CaCO3反应生成CaCl2、CO2和H2O,所以加入盐酸可除去CaCO3。
③Fe与FeCl3反应生成FeCl2,所以加入Fe可除去FeCl3。
④加入盐酸生成无色无味气体的溶液是Na2CO3,生成无色刺激性气味气体的溶液是Na2SO3,生成白色沉淀的溶液是Na2SiO3。
⑤加入Ba(OH)2溶液,只生成白色沉淀的溶液是Na2SO4,只生成刺激性气味气体的溶液是NH4Cl,既生成白色沉淀,也生成刺激性气味气体的溶液是(NH4)2SO4.
(2)化合反应与分解反应部分属于氧化反应,部分属于非氧化反应;类型Ⅲ为复分解反应,生成H2O的反应都可以,如酸碱中和反应:HCl+NaOH=NaCl+H2O;反应类型Ⅳ是置换反应,有H2O参加反应如:2Na+2H2O=2NaOH+H2↑,水为氧化剂。
(3)Cl2与SO2、H2O反应生成H2SO4和HCl,离子方程式为:SO2+C12+2H2O===4H++SO42-+2Cl-
考点:本题考查物质的鉴别和除杂、基本反应类型与氧化还原反应、离子方程式的书写。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案