题目内容
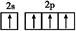
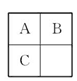
A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大。A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y );D形成的分子为双原子分子。回答问题:
(1)D元素的名称为 , F形成的离子的结构示意图为 。
(2)写出液态化合物Y的一种用途 。
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式 ________ ,使用这种气球存在的隐患是 。
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应。写出该反应的离子方程式: 。
(5)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为 。
(1)D元素的名称为 , F形成的离子的结构示意图为 。
(2)写出液态化合物Y的一种用途 。
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式 ________ ,使用这种气球存在的隐患是 。
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应。写出该反应的离子方程式: 。
(5)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为 。
(1)氟 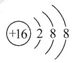
(2)一定浓度的H2O2溶液作消毒剂
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑ 易燃、易爆
(4)H++HSO3-=SO2↑+H2O
(5)NH3+HCl=NH4Cl
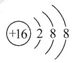
(2)一定浓度的H2O2溶液作消毒剂
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑ 易燃、易爆
(4)H++HSO3-=SO2↑+H2O
(5)NH3+HCl=NH4Cl
E原子半径在短周期主族元素中最大,E为Na;A与E最外层电子数相同,A、E同主族,A为H;C元素在第二周期,H元素与C元素形成两种常见的液态化合物,C为氧元素;F质子数是C的2倍,F为S;B、C同周期且相邻,B为N;D为F;G为Cl。
(1)D元素名称为氟,S2-的结构示意图为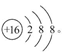
(2)化合物Y为H2O2,可以作医用消毒剂和漂白剂等。
(3)Al与NaOH溶液反应产生H2,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。氢气球存在的问题是易燃、易爆。
(4)H、O、Na、S形成的化合物都显酸性,则为NaHSO4和NaHSO3,反应的离子方程式为:H++HSO3-=SO2↑+H2O。
(5)H、N、Cl三种元素形成的NH3与HCl反应的化学方程式为:NH3+HCl=NH4Cl。
(1)D元素名称为氟,S2-的结构示意图为
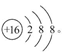
(2)化合物Y为H2O2,可以作医用消毒剂和漂白剂等。
(3)Al与NaOH溶液反应产生H2,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。氢气球存在的问题是易燃、易爆。
(4)H、O、Na、S形成的化合物都显酸性,则为NaHSO4和NaHSO3,反应的离子方程式为:H++HSO3-=SO2↑+H2O。
(5)H、N、Cl三种元素形成的NH3与HCl反应的化学方程式为:NH3+HCl=NH4Cl。

练习册系列答案
相关题目