题目内容
(12分)(1) 0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5千焦热量,其热化学方程式是:
。
又已知:H2O(液)=H2O(气);△H =-44kJ/mol,则11.2升(标准状况下)乙硼烷完全燃烧时生成气态水时放出的热量为 千焦。
(2)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态 水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________ ________________。
水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为________________ ________________。
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。
(12分)
(1)B2H6(g)+3O2(g)→B2O3(s)+3H2O(l) ΔH=–2165.0kJ·mol-1; 1016.5
(2)CH3OH(l)+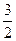 O2(g)→CO2(g)+2H2O(l) ΔH=–725.76kJ·mol-1
O2(g)→CO2(g)+2H2O(l) ΔH=–725.76kJ·mol-1
(3)N2(g)+3H2(g) === 2NH3(g) ΔH=-92kJ·mol-1
解析

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
(双选).在密闭容器中进行反应X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol.L-1、0.3mol.L-1、0.2mol.L-1,在一定条件下当反应达到平衡时,各物质的浓度有可能是( )
| A、Z为0.3mol.L-1, | B、X2为0.2mol.L-1, | C、Y2为0.3mol.L-1, | D、Z为0.4mol.L-1, |