题目内容
【题目】某学习小组为研究电化学原理,设计右图装置。下列叙述正确的是( )
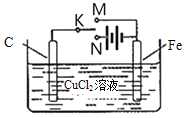
A. K与M相连时,每转移1mol电子Fe表面生成32gCu
B. K与N相连时,碳棒上产生使湿润的淀粉-KI试纸变蓝的气体
C. K分别与M、N相连时,铁均受到保护
D. K与M、N均断开,一段时间后电解质溶液质量变大
【答案】B
【解析】A,K与M相连时,装置为原电池,Fe为负极,Fe极的电极反应式为Fe-2e-=Fe2+,C为正极,C极的电极反应式为Cu2++2e-=Cu,Cu在C表面析出,A项错误;B,K与N相连时,装置为电解池,Fe为阴极,C为阳极,C极的电极反应式为2Cl--2e-=Cl2↑,Cl2能使湿润的淀粉-KI试纸变蓝,B项正确;C,K与M相连时,Fe为原电池的负极,Fe的腐蚀加快,C项错误;D,K与M、N均断开,发生反应Fe+CuCl2=FeCl2+Cu,一段时间后电解质溶液质量变小,D项错误;答案选B。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是___________。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
② | 在FeCl2溶液中加入锌片 |
| Zn+Fe2+=Zn2++Fe | |
③ | 在FeCl3溶液中加入足量铁粉 |
| Fe+2Fe3+=3 Fe2+ | Fe3+具有氧化性 |
④ |
|
| Fe3+具有氧化性 |
实验结论:_________________________________。
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:_____。(填序号)
A、Cl2 B、Na C、Na+ D、Cl- E、SO2 F、盐酸