题目内容
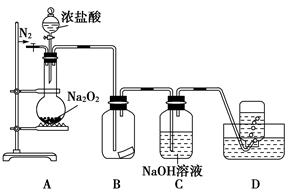
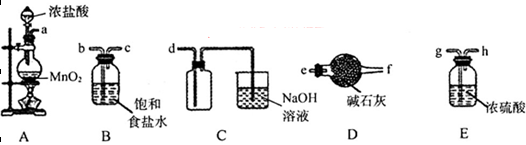
无水氯化亚铁用于制造铁系催化剂、印染的媒染剂和染料还原剂,还可用于冶金、医药、照相等行业。一实验小组模仿工业方法制取氯化亚铁,设计装置如下

通过查阅相关资料可知:
①在持续高温500℃时,铁与纯净、干燥Cl2反应可生成FeCl2,在温度较低时可生成FeCl3;
②FeCl3熔沸点低,易升华。
根据以上信息回答相关的问题
(1)abc仪器组合成制取氯气的装置,反应无需加热,请写出a容器内所发生的化学反应方程式 。
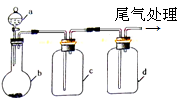
(2)d、e盛装的药品分别是 和 ,f、g的作用是 。
(3)反应器为硬质玻璃管,纯净铁粉与氯气在500℃左右反应。
①化学反应方程式为
②实验操作顺序是:组装仪器、 、装入药品、 、 、停止加热、关闭c的活塞。
(4)实验小组记录的实验现象如下:
①第一次实验,发现e瓶没有盛装任何药品,所以得到红色固体,其原因是 。
②第二次实验,g瓶有红棕色的烟,其原因是 。
(5)第三次实验得到的固体,最可能含有微量杂质是 ,如果需要配制约2~3mol/L的染料还原剂溶液,则无需除去,理由是 。

通过查阅相关资料可知:
①在持续高温500℃时,铁与纯净、干燥Cl2反应可生成FeCl2,在温度较低时可生成FeCl3;
②FeCl3熔沸点低,易升华。
根据以上信息回答相关的问题
(1)abc仪器组合成制取氯气的装置,反应无需加热,请写出a容器内所发生的化学反应方程式 。
(2)d、e盛装的药品分别是 和 ,f、g的作用是 。
(3)反应器为硬质玻璃管,纯净铁粉与氯气在500℃左右反应。
①化学反应方程式为
②实验操作顺序是:组装仪器、 、装入药品、 、 、停止加热、关闭c的活塞。
(4)实验小组记录的实验现象如下:
| | 观察到的部分现象 |
| 第一次实验 | 反应器中有白雾、红色固体、g瓶有白雾和黄绿色气体 |
| 第二次实验 | 反应器中有绿色晶体,g瓶有红棕色的烟和黄绿色气体 |
| 第三次实验 | 反应器中有绿色晶体,g瓶有黄绿色气体 |
①第一次实验,发现e瓶没有盛装任何药品,所以得到红色固体,其原因是 。
②第二次实验,g瓶有红棕色的烟,其原因是 。
(5)第三次实验得到的固体,最可能含有微量杂质是 ,如果需要配制约2~3mol/L的染料还原剂溶液,则无需除去,理由是 。
(1)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O (用次氯酸盐也可)
(2)饱和食盐水、浓硫酸 安全、防止倒吸
(3) ①Fe+Cl2 FeCl2 ②检验装置的气密性、先加热、 再打开c的活塞
FeCl2 ②检验装置的气密性、先加热、 再打开c的活塞
(4)①氯气没有干燥,生成的盐发生水解,生成了氢氧化物,最终分解得到三氧化二铁
②加热时温度没有维持至500℃左右,在温度较低时生成了氯化铁,由于氯化铁熔沸点低,受热时变成气体进入在g瓶中
(5)铁单质 铁单质可以防止Fe2+被氧化
(2)饱和食盐水、浓硫酸 安全、防止倒吸
(3) ①Fe+Cl2
 FeCl2 ②检验装置的气密性、先加热、 再打开c的活塞
FeCl2 ②检验装置的气密性、先加热、 再打开c的活塞 (4)①氯气没有干燥,生成的盐发生水解,生成了氢氧化物,最终分解得到三氧化二铁
②加热时温度没有维持至500℃左右,在温度较低时生成了氯化铁,由于氯化铁熔沸点低,受热时变成气体进入在g瓶中
(5)铁单质 铁单质可以防止Fe2+被氧化
|
 FeCl2。②有气体参加的反应或制取气体的反应,在实验前一定要先检查装置的气密性,然后再进行实验。实验操作顺序是:组装仪器、检验装置的气密性、活塞、装入药品、先加热、再打开c的活塞、停止加热、关闭c的活塞。(4)①第一次实验,发现e瓶没有盛装任何药品,则氯气没有干燥,生成的盐发生水解,首先生成了氢氧化亚铁,在空气中被氧化为氢氧化铁,在灼烧时发生分解反应,最终得到红棕色的三氧化二铁。②第二次实验,加热时温度没有维持至500℃左右,在温度较低时生成了氯化铁,由于氯化铁熔沸点低,受热时变成气体进入在g瓶中,使g瓶有红棕色的烟。(5)第三次实验得到的固体,最可能含有微量杂质是金属Fe的单质。如果需要配制约2~3mol/L的染料还原剂溶液,由于Fe2+容易被空气中的氧气氧化,而铁单质可以防止Fe2+被氧化,因此该杂质无需除去。考点:
FeCl2。②有气体参加的反应或制取气体的反应,在实验前一定要先检查装置的气密性,然后再进行实验。实验操作顺序是:组装仪器、检验装置的气密性、活塞、装入药品、先加热、再打开c的活塞、停止加热、关闭c的活塞。(4)①第一次实验,发现e瓶没有盛装任何药品,则氯气没有干燥,生成的盐发生水解,首先生成了氢氧化亚铁,在空气中被氧化为氢氧化铁,在灼烧时发生分解反应,最终得到红棕色的三氧化二铁。②第二次实验,加热时温度没有维持至500℃左右,在温度较低时生成了氯化铁,由于氯化铁熔沸点低,受热时变成气体进入在g瓶中,使g瓶有红棕色的烟。(5)第三次实验得到的固体,最可能含有微量杂质是金属Fe的单质。如果需要配制约2~3mol/L的染料还原剂溶液,由于Fe2+容易被空气中的氧气氧化,而铁单质可以防止Fe2+被氧化,因此该杂质无需除去。考点:
练习册系列答案
相关题目
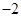 价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:
价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下: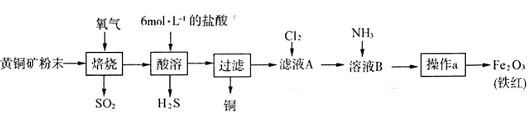
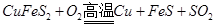
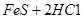 =
=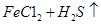
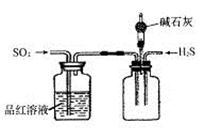
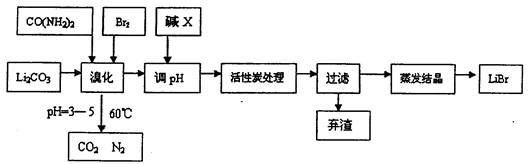
 6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下:
6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下: