题目内容
【题目】十九大报告指出,“建设生态文明是中华民族水续发展的千年大计”。控制和治理NOx、SO2、CO2是解决光化学烟算、减少酸雨和温室效应的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
(1)利用SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
①SCR(选择催化还原NOx)工作原理:
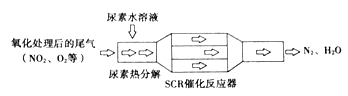
尿素水溶液热分解为NH3和CO2的化学方程式为________,SCR催化反应器中NH3还原NO2的化学方程式为__________。
②NSR(NOx储存还原)工作原理:
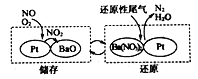
在储存过程中,NO发生的总化学反应方程式为__________
(2)双碱法除去SO2的工作原理:NaOH溶液![]() Na2SO3溶液
Na2SO3溶液
过程①的离子方程式为_____;CaO在水中存在如下转化:CaO(s)+H2O(1)=Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②NaOH再生的原理____________.
Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②NaOH再生的原理____________.
(3)人工光合作用技术回收利用二氧化碳的工作原理:
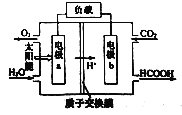
a极为_______极,b极的电极反应式为______________。
【答案】 CO(NH2)2+H2O![]() CO2+2NH3 8NH3+6NO2
CO2+2NH3 8NH3+6NO2![]() 7N2+12H2O 2BaO+4NO+3O2
7N2+12H2O 2BaO+4NO+3O2![]() 2Ba(NO3)2 2OH-+SO2=SO32-+H2O SO32-与Ca2+生成CaSO3沉淀,平衡正向移动,有NaOH生成 负 CO2+2H++2e-=HCOOH
2Ba(NO3)2 2OH-+SO2=SO32-+H2O SO32-与Ca2+生成CaSO3沉淀,平衡正向移动,有NaOH生成 负 CO2+2H++2e-=HCOOH
【解析】(1)①根据原子守恒可知尿素水溶液热分解为NH3和CO2的化学方程式为CO(NH2)2+H2O![]() CO2+2NH3;SCR催化反应器中NH3还原NO2生成氮气和水的化学方程式为8NH3+6NO2
CO2+2NH3;SCR催化反应器中NH3还原NO2生成氮气和水的化学方程式为8NH3+6NO2![]() 7N2+12H2O。②根据示意图可知在储存过程中NO在催化剂的作用下转化为硝酸钡,因此发生的总化学反应方程式为2BaO+4NO+3O2
7N2+12H2O。②根据示意图可知在储存过程中NO在催化剂的作用下转化为硝酸钡,因此发生的总化学反应方程式为2BaO+4NO+3O2![]() 2Ba(NO3)2;(2)过程①是氢氧化钠溶液吸收SO2转化为亚硫酸钠,反应的离子方程式为2OH-+SO2=SO32-+H2O;由于溶液中的SO32-与Ca2+结合生成CaSO3沉淀,使平衡正向移动,因此有NaOH生成;(3)a极产生氧气,说明是氢氧根发生失去电子的氧化反应,则a极为负极;b极是正极,CO2得到电子结合氢离子转化为甲酸,电极反应式为CO2+2H++2e-=HCOOH。
2Ba(NO3)2;(2)过程①是氢氧化钠溶液吸收SO2转化为亚硫酸钠,反应的离子方程式为2OH-+SO2=SO32-+H2O;由于溶液中的SO32-与Ca2+结合生成CaSO3沉淀,使平衡正向移动,因此有NaOH生成;(3)a极产生氧气,说明是氢氧根发生失去电子的氧化反应,则a极为负极;b极是正极,CO2得到电子结合氢离子转化为甲酸,电极反应式为CO2+2H++2e-=HCOOH。