题目内容
【题目】氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成都需要用它。
(1)工业上通常采用电解法制氯气,请观察图后回答下列问题:
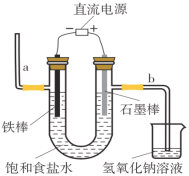
① 请写出该反应的化学方程式________________________________。
② 通电后,b侧产生的气体是______![]() 填化学式
填化学式![]() 。
。
(2)某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉![]() 这是一个放热反应
这是一个放热反应![]() ,回答下列问题:
,回答下列问题:
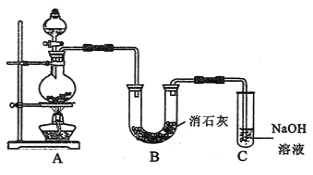
①在A装置中用固体二氧化锰与浓盐酸,在加热条件下制取氯气,请写出反应的化学方程式________________________________。
②漂白粉将在U形管中产生,其化学方程式是______________________________。
③装置C的作用是______________。
④此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
I.温度较高时氯气与消石灰反应生成![]() ,为避免此副反应的发生,可采取的措施是________________________。
,为避免此副反应的发生,可采取的措施是________________________。
II.试判断另一个副反应![]() 用化学方程式表示
用化学方程式表示![]() ______________________________,为避免此副反应的发生,可以在A与B之间连接一个装有______的洗气瓶。
______________________________,为避免此副反应的发生,可以在A与B之间连接一个装有______的洗气瓶。
【答案】2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ Cl2 MnO2+4HCl(浓)
2NaOH+H2↑+Cl2↑ Cl2 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O; 吸收未反应完的氯气,防止污染空气 冷却B装置 2HCl+Ca(OH)2=CaCl2+2H2O 饱和氯化钠溶液
MnCl2+Cl2↑+2H2O Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O; 吸收未反应完的氯气,防止污染空气 冷却B装置 2HCl+Ca(OH)2=CaCl2+2H2O 饱和氯化钠溶液
【解析】
(1)①电解饱和食盐水可以得到氢氧化钠、氯气和氢气;
②b侧产生的气体是氯气,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
(2)①Mn元素化合价由+4价降低到+2价,Cl元素化合价由-1价升高到0价,根据化合价的升降相等配平方程式;
②氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水;
③氯气有毒,不能直接排放到空气中,需要进行尾气吸收;
④I.依据信息可知温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生应降低温度;
II.盐酸易挥发,会与消石灰反应,在A与B之间连接一个装有饱和食盐水的洗气瓶。
(1)①电解饱和食盐水可以得到氢氧化钠、氯气和氢气,化学方程式是:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
答案:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
②b侧电极是阳极,氯离子放电,产生的气体是氯气,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
答案:Cl2
(2)①Mn元素化合价由+4价降低到+2价,Cl元素化合价由-1价升高到0价,根据化合价的变化配平方程式,MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
答案:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②氯气与氢氧化钙反应生成氯化钙、次氯酸钙和水,化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
答案:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
③氯气有毒,不能直接排放到空气中,需要进行尾气吸收;
答案:吸收未反应完的氯气,防止污染空气
④I.依据信息可知温度较高时氯气与消石灰反应生成Ca(ClO3)2,为为避免此副反应的发生应降低温度;
答案:冷却B装置
II.盐酸易挥发,会与消石灰反应:2HCl+Ca(OH)2=CaCl2+2H2O,可以在A与B之间连接一个装有饱和食盐水的洗气瓶;
答案:2HCl+Ca(OH)2=CaCl2+2H2O 饱和氯化钠溶液
