题目内容
【题目】如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是( )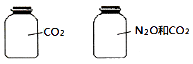
A.所含氧原子数相等
B.气体的总质量相等
C.气体所含电子总数相等
D.气体的密度相等
【答案】A
【解析】同温同压下,体积之比等于物质的量之比,两瓶气体的物质的量相等,
A.N2O和CO2含有的O原子数目不同,则两个集气瓶中含有O原子的物质的量不同,含有氧原子数不同,A符合题意;
B.N2O和CO2的摩尔质量都是44g/mol,两瓶气体的物质的量相等,根据m=nM可知气体的总质量相等,B不符合题意;
C.N2O和CO2都含有22个电子,两瓶气体的物质的量相等,则含有电子数相等,C不符合题意;
D.N2O和CO2的摩尔质量都是44g/mol,根据ρ= ![]() 可知,相同条件下两瓶气体的密度相等,D不符合题意;
可知,相同条件下两瓶气体的密度相等,D不符合题意;
故答案为:A.
根据阿佛加德罗定律:同温同压下,体积相等,则两瓶气体的物质的量相等;A.N2O和CO2分子中含有的O原子数目不同,分子物质的量相同时氧原子的物质的量不同;B.N2O和CO2的摩尔质量相同,两气体的物质的量相等,质量相等;C.N2O和CO2为等电子体,物质的量相等,则含有电子数相等;D.ρ= ![]() 可知,相同条件下气体摩尔质量相等则密度相等。
可知,相同条件下气体摩尔质量相等则密度相等。

练习册系列答案
相关题目