题目内容
【题目】海水是巨大的资源宝库。
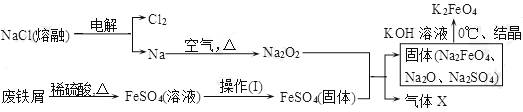
Ⅰ.从海水中提取食盐和溴(海水中溴以溴化钠为主)的过程如下:

(1)步骤①工业上得到氯气的化学方程式为:_______________________________________________。
(2)步骤②的化学方程式为:________________________________________________。
(3)步骤③用SO2水溶液吸收Br2,可制得HBr和硫酸,离子方程式为:________________________。
Ⅱ.海洋植物如海带、海藻中含有丰富的碘元素,燃烧的灰烬中碘元素以I-的形式存在。实验室里从海藻中提取碘的流程如下:

(4)指出提取碘的过程中有关的实验操作名称:
①______________ ③______________ ④______________
(5)步骤③操作所需的玻璃仪器主要是______________________。
(6)提取碘的过程中,可供选择的有机试剂是______(填字母)。
A.苯、酒精 B.汽油、醋酸 C.四氯化碳、苯
【答案】 2NaCl+ 2H2O![]() H2↑+Cl2↑+2NaOH Cl2+2NaBr=Br2+2NaCl Br2+SO2+2H2O=4H+ +2Br -+SO42- 过滤 萃取(分液) 蒸馏 分液漏斗 C
H2↑+Cl2↑+2NaOH Cl2+2NaBr=Br2+2NaCl Br2+SO2+2H2O=4H+ +2Br -+SO42- 过滤 萃取(分液) 蒸馏 分液漏斗 C
【解析】Ⅰ.(1)步骤①中工业上通过电解饱和食盐水生产氯气,反应的化学方程式为2NaCl+ 2H2O![]() H2↑+Cl2↑+2NaOH,故答案为:2NaCl+ 2H2O
H2↑+Cl2↑+2NaOH,故答案为:2NaCl+ 2H2O![]() H2↑+Cl2↑+2NaOH;
H2↑+Cl2↑+2NaOH;
(2)步骤②中氯气与母液中的溴化钠反应置换出溴,反应的化学方程式为Cl2+2NaBr=Br2+2NaCl,故答案为:Cl2+2NaBr=Br2+2NaCl;
(3)二氧化硫吸收溴单质发生反应:Br2+SO2+2H2O═4H++SO42-+2Br-;故答案为:Br2+SO2+2H2O═4H++SO42-+2Br-;
Ⅱ.(4)根据流程图,操作①是分离固体和溶液,为过滤;操作③是从碘水中提取碘,为萃取和分液;操作④是从萃取后的有机层中获得碘,为蒸馏,故答案为:过滤;萃取、分液;蒸馏;
(5)步骤③为萃取,用到的玻璃仪器主要是分液漏斗,故答案为:分液漏斗;
(6)萃取的基本原则两种溶剂互不相溶。酒精、醋酸和水互溶,不能用作萃取剂,苯、四氯化碳、汽油与水互不相容,可用作萃取剂,故答案为:C。

【题目】已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行氯气的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是
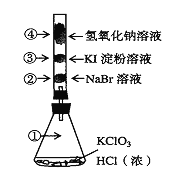
① | ② | ③ | ④ | |
A | 黄绿色 | 橙色 | 蓝色 | 无色 |
B | 无色 | 橙色 | 紫色 | 白色 |
C | 黄绿色 | 橙色 | 蓝色 | 白色 |
D | 黄绿色 | 无色 | 紫色 | 白色 |