题目内容
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项事实不能说明上述观点的是( )
| A.乙酸分子中羟基上的氢原子较乙醇中羟基上的氢原子更活泼 |
| B.乙炔能发生加成反应,而乙烷不能发生加成反应 |
| C.甲苯的硝化反应较苯更容易 |
| D.苯酚能和氢氧化钠溶液反应,而乙醇不能和氢氧化钠溶液反应 |
B
A正确,乙酸分子中羟基上的氢原子因受羰基的影响,更易电离出氢,而乙醇分子中羟基上的氢受乙基的影响不大,难电离出氢;B错,乙炔能发生加成反应是因为分子结构中存在碳碳三键;乙烷为饱和烃不能加成;C正确,甲苯中苯环受甲基的影响,使得苯环上甲基的邻、对位C上的氢更易被取代;D正确,苯酚溶液显弱酸性是苯环影响羟基,使得羟基上的氢更易电离,而乙醇仅受乙基的影响,且影响效果很弱;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 =”),基态C原子的电子排布式为 。
=”),基态C原子的电子排布式为 。
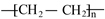
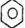 ③CH3CH2OH ④CH3COOH⑤聚乙烯五种物质中:
③CH3CH2OH ④CH3COOH⑤聚乙烯五种物质中: 的是 ;
的是 ;