题目内容
加0.1 mol MnO2粉末于50 mL过氧化氢(H2O2,ρ=1.1 g· mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。
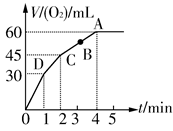
(1)实验时放出气体的总体积是_____________________________。
(2)放出一半气体所需时间为_______________________________。
(3)反应放出气体总体积的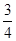 所需的时间约为__________________
所需的时间约为__________________
(4)A、B、C、D各点反应速率快慢的顺序为____________________
(5)解释反应速率变化的原因___________________________________________________
(6)计算H2O2的初始物质的量浓度____________________
(7)求反应到2 min时,H2O2的质量分数_________________________

(1)实验时放出气体的总体积是_____________________________。
(2)放出一半气体所需时间为_______________________________。
(3)反应放出气体总体积的
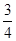 所需的时间约为__________________
所需的时间约为__________________(4)A、B、C、D各点反应速率快慢的顺序为____________________
(5)解释反应速率变化的原因___________________________________________________
(6)计算H2O2的初始物质的量浓度____________________
(7)求反应到2 min时,H2O2的质量分数_________________________
(1)60 mL (2)1 min (3)2 min (4)D>C>B>A
(5)随着反应的进行,c(H2O2)逐渐降低,反应逐渐变慢
(6)0.107 mol·L-1 (7)0.084%
(5)随着反应的进行,c(H2O2)逐渐降低,反应逐渐变慢
(6)0.107 mol·L-1 (7)0.084%
根据V-t图像知,反应进行至1 min时,放出O2的体积为30 mL,反应进行至2 min时,放出O2 45 mL,反应进行至4 min,放出O2的体积达最大值60 mL;由V-t曲线的斜率变化可知:D、C、B、A的反应速率逐渐减小,这是因为随着反应的进行,c(H2O2)逐渐降低,反应逐渐变慢;根据2H2O2 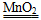 2H2O+O2↑,n(H2O2)=
2H2O+O2↑,n(H2O2)= 
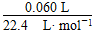 ×2,所以H2O2的起始物质的量浓度为:
×2,所以H2O2的起始物质的量浓度为: 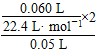 =0.107 mol·L-1;反应进行至2 min时,消耗H2O2的物质的量为
=0.107 mol·L-1;反应进行至2 min时,消耗H2O2的物质的量为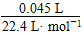 ×2=0.004 mol,剩余H2O2的物质的量为
×2=0.004 mol,剩余H2O2的物质的量为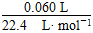 ×2-0.004 mol=1.36×10-3 mol。
×2-0.004 mol=1.36×10-3 mol。
所以w(H2O2)=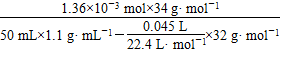 ×100%≈0.084%。
×100%≈0.084%。
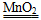 2H2O+O2↑,n(H2O2)=
2H2O+O2↑,n(H2O2)= 
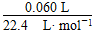 ×2,所以H2O2的起始物质的量浓度为:
×2,所以H2O2的起始物质的量浓度为: 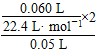 =0.107 mol·L-1;反应进行至2 min时,消耗H2O2的物质的量为
=0.107 mol·L-1;反应进行至2 min时,消耗H2O2的物质的量为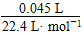 ×2=0.004 mol,剩余H2O2的物质的量为
×2=0.004 mol,剩余H2O2的物质的量为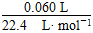 ×2-0.004 mol=1.36×10-3 mol。
×2-0.004 mol=1.36×10-3 mol。所以w(H2O2)=
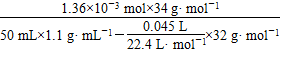 ×100%≈0.084%。
×100%≈0.084%。
练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
 CH3OH(g)+ H2O(g)△H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是
CH3OH(g)+ H2O(g)△H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是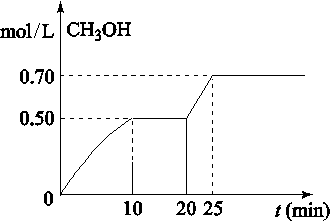
 2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1,对此反应速率的表示正确的是( )
2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1,对此反应速率的表示正确的是( ) 2C(g),在10s内反应物A的浓度由1mol/L降到0.4mol/L,则ν(C)为
2C(g),在10s内反应物A的浓度由1mol/L降到0.4mol/L,则ν(C)为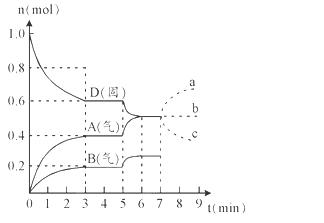
 2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)
2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B) cC(g);5min时,测得C为xmol。下列说法中一定正确的是( )
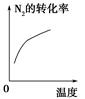
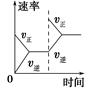
cC(g);5min时,测得C为xmol。下列说法中一定正确的是( ) 2NH3(g);ΔH<0,下列研究目的和示意图相符的是 ( )。
2NH3(g);ΔH<0,下列研究目的和示意图相符的是 ( )。
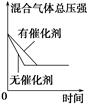
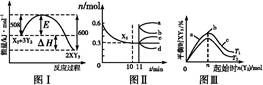
 2XY3(g)。图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2 L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响。
2XY3(g)。图Ⅰ表示在一定温度下此反应过程中的能量变化;图Ⅱ表示在2 L的密闭容器中反应时X2的物质的量随时间的变化曲线;图Ⅲ表示在其他条件不变的情况下,改变起始物Y2的物质的量对此反应平衡的影响。