题目内容
【题目】(1)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:

①该反应在_________min时达到化学平衡状态。
②该反应的化学方程式是______________________。
③从开始到2min,Z的平均反应速率是________________________。
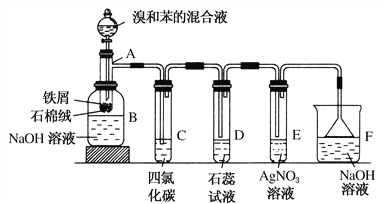
(2)某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题:

①若a、b是两种活动性不同的金属,则活动性a____b(填>、<或=);
②电路中的电子从____经导线流向_____(填a或b);
③溶液中的SO42-向________极移动(填a或b);
④若两电极分别是Al和C,则负极的电极反应式为_________________。
(3)将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题:

通入甲醇的电极是_____(填“正”或“负”)极,反应时该电极附近的现象是_____________________________,溶液中K+向____(填“正”或“负”)极移动:写出正极反应式:_______________;若电池工作过程中通过2mol电子,则理论上消耗O2__L(标准状况)。
【答案】 2 3X+Y![]() 2Z 0.05mol·(L-1·min-1) < b a b Al-3e-=Al3+ 负 【答题空10】溶液红色变浅(答褪色不得分) 正 O2+4e-+2H2O=4OH- 11.2L
2Z 0.05mol·(L-1·min-1) < b a b Al-3e-=Al3+ 负 【答题空10】溶液红色变浅(答褪色不得分) 正 O2+4e-+2H2O=4OH- 11.2L
【解析】(1)①可逆反应达到平衡状态时,各物质的物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的一系列物理量不变,根据图知,当2min时各物质的物质的量不变,则此时该反应达到平衡状态,故答案为:2;
②同一可逆反应同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,根据图知,该反应中参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,则X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,则该反应方程式为3X+Y![]() 2Z,故答案为:3X+Y
2Z,故答案为:3X+Y![]() 2Z;
2Z;
③v(Z)=![]() =
=![]() =0.05mol/(L.min),故答案为:0.05mol/(L.min);
=0.05mol/(L.min),故答案为:0.05mol/(L.min);
(2)原电池中活泼性强的为负极,正极上溶液中的阳离子得电子,a极上有红色金属析出,则a为正极,b为负极。
①若a、b是两种活动性不同的金属,a为正极,b为负极,则活动性a<b;故答案为:<;
②放电时,电子从负极流向正极,则电路中的电子从b经导线流向 a;故答案为:b;a;
③溶液中阴离子向负极移动,所以溶液中的SO42-向 b移动;故答案为:b;
④若两电极分别是Al和C,Al为负极,负极上铝失电子生成铝离子,则负极的电极反应式为Al-3e-=Al3+;故答案为:Al-3e-=Al3+;
(3)通入甲醇的电极是负极,反应时该电极反应:CH3OH+8OH--6e-=CO32-+6H2O,故溶液红色变浅;该燃料电池工作时,阳离子向正极移动,氧气在碱性电解质溶液中得电子,所以电池正极的电极反应式为:O2+2H2O+4e-=4OH-,电池工作过程中通过2mol电子,则理论上消耗O2的体积=![]() ×22.4L/mol=11.2L,故答案为:负;溶液红色变浅;正;O2+2H2O+4e-=4OH-;11.2L。
×22.4L/mol=11.2L,故答案为:负;溶液红色变浅;正;O2+2H2O+4e-=4OH-;11.2L。

【题目】以硼镁泥(主要成分为MgSiO3、Fe2O3及少量Al2O3、FeO和MnO)为原料制备高纯Mg(OH)2的流程如下:
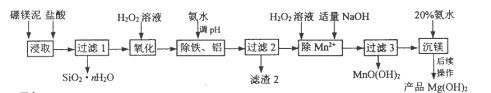
己知:
①常温下此体系中各氢氧化物开始沉淀与沉淀完全时的pH范围如下表所示:
pH值 | Mg(OH)2 | Mn(OH)2 | MnO(OH)2 | Fe(OH)2 | Al(OH)3 | Fe(OH)3 |
开始沉淀时 | 9.3 | 7.1 | 7.8 | 7.6 | 3.7 | 2.3 |
沉淀完全时 | 10.8 | 10.8 | 9.8 | 9.6 | 4.7 | 3.7 |
②温度高于340℃时Mg(OH)2开始分解为MgO和H2O。
(1)“浸取”时,为提高镁的浸取率可行的措施为__________。
a.将硼镁泥制成浆料 b.降低浸取温度 c.用盐酸多次浸取
(2)“浸取”时,MgSiO3与盐酸反应的化学方程式为_________________________。
(3)“除铁、铝”时,需调节溶液pH范围为_________________________。
(4)“除Mn2+”时发生反应的离子方程式为_________________________;
过滤3所得滤渣中含有MnO(OH)2和__________。
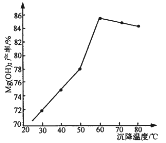
(5)“沉镁”时,反应温度与Mg(OH)2的产率如图所示,当温度超过60℃,随温度再升高,Mg(OH)2产率反而降低,其原因可能是________________。