题目内容
【题目】【加试题】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。请回答:
(1)已知:2Al2O3(s)===4Al(g)+3O2(g) ΔH1=3351 kJ·molˉ1
2C(s)+O2(g)===2CO(g) ΔH2=-221 kJ·molˉ1
2Al(g)+N2(g)===2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成AlN的总热化学方程式是 , 该反应自发进行的条件 。
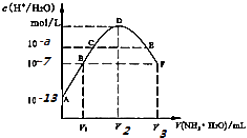
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应Ⅰ CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) ΔH4
CH4(g)+2H2O(g) ΔH4
反应Ⅱ CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5
①下列说法不正确的是
A.ΔH 4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为V L,该温度下反应Ⅰ的平衡常数为(用a、V表示)
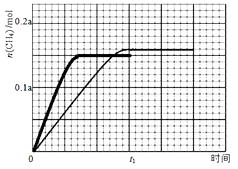
(3)350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。
(4)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是 。
【答案】
(1)Al2O3(s)+ 3C(s)+ N2(g)===2Al(g) +3CO(g)+ 2AlN(s),ΔH=+1026 kJ·molˉ1;高温
(2)CD;625V2/a2
(3)
(4)CO2+ 6H2O +8eˉ === 6CH4+ 8OHˉ
【解析】解:(1) 通过观察已知三个方程式,用Al2O3合成AlN的方程式为
Al2O3(s)+3C(s)+N2(g)===2Al(g)+3CO(g)+2AlN(s),ΔH=(ΔH1+3ΔH2+2ΔH3)/2=+1026kJ·molˉ1 , 又∵ΔS>0,∴高温自发
由图一转化率随温度变化看出,350℃之前为未平衡之前的转化率,之后为CO2的平衡转化率,温度升高转化率降低,说明反应Ⅰ为放热反应A正确,C错误;从图2可以看出温度对生成产物(产物的选择性)有影响,B正确;相同条件下CO2和H2的初始体积比从1:4改变为1∶3,前者CO2的转化率高,D错误;故选择C、D
根据图一350℃ CO2的平衡转化率为0.8,三段式进行计算
CO2(g)+ | 4H2(g) | CH4(g)+ | 2H2O(g) | |
初n |
|
| 0 | 0 |
转化n |
|
|
|
|
平衡n |
|
|
|
|
代入求平衡常数K=[ ![]() a ×0.8×(
a ×0.8×( ![]() a ×1.6)2×
a ×1.6)2× ![]() ]/[
]/[ ![]() a ×0.2×(
a ×0.2×( ![]() a ×0.8)4×
a ×0.8)4× ![]() ]=625V2/a2
]=625V2/a2
(要除以体积转化为浓度之后代入)
t1时350℃达到平衡,反应为放热反应,400℃反应速率加快,平衡逆移动,后生成甲烷的量减少。