题目内容
在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答: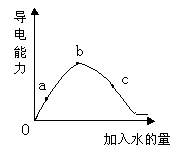
⑴“O”点导电能力为0的理由是: 。
⑵a、b、c三点溶液中,[H+]由小到大的顺序是: 。
⑶a、b、c三点溶液中,醋酸的电离程度最大的是: 。
⑷若使c点溶液中[CH3COO-]增大,而[H+]减小,可采取的措施主要有:① ;② ;③ ;④ 。

⑴“O”点导电能力为0的理由是: 。
⑵a、b、c三点溶液中,[H+]由小到大的顺序是: 。
⑶a、b、c三点溶液中,醋酸的电离程度最大的是: 。
⑷若使c点溶液中[CH3COO-]增大,而[H+]减小,可采取的措施主要有:① ;② ;③ ;④ 。
⑴冰醋酸未电离,其中没有自由移动的离子;⑵c<a<b;⑶c;⑷①CH3COOH;②NaOH;③Na2CO3;④Mg。
⑴冰醋酸未电离,其中没有自由移动的离子;⑵导电能力越强,自由移动的离子浓度越大,故[H+]由小到大的顺序是c<a<b;⑶随着加水的量的增加,将促进醋酸的电离,故c点醋酸的电离程度最大;⑷使醋酸溶液中的CH3COO-溶液增大,可加入物质与H+反应使醋酸电离平衡向电离的方向移动,如氢氧化钠、碳酸钠及金属镁;而加入醋酸钠,虽使醋酸电离平衡向左移动,但剩余的CH3COO-的浓度仍是增加的,所以加入醋酸钠也符合题意。

练习册系列答案
相关题目
 H++HS-;第二步:HS-
H++HS-;第二步:HS-