题目内容
【题目】镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运及污染小等特点。如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是
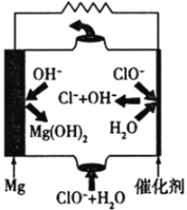
A. 该燃料电池中镁为负极,发生氧化反应
B. 正极反应式为ClO―+H2O+2e―=Cl―+2OH―
C. 放电过程中OH―移向正极移动
D. 电池总反应式为Mg+ClO―+H2O=Mg(OH)2+Cl―
【答案】C
【解析】
该燃料电池中,镁易失电子作负极、次氯酸根离子得电子发生还原反应,结合原电池的工作原理显解答。
A.镁失电子发生氧化反应而作负极,故A正确;
B.正极上双氧水得电子发生还原反应,电极反应式为正极反应式为ClO―+H2O+2e―=Cl―+2OH―,故B正确;
C.放电过程中阴离子氢氧根离子向负极移动,故C错误;
D.镁在负极上失电子生成镁离子,次氯酸根离子在正极上得电子和水生成氯离子和氢氧根离子,所以电池反应式为Mg+ClO―+H2O=Mg(OH)2+Cl―,故D正确;
答案选C。

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目