题目内容
5.以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,违反了泡利原理的是②,违反了洪特规则的是③⑤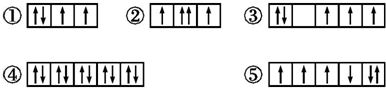
分析 泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;
洪特规则:在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同,以此进行判断.
解答 解:①2p能层有4个电子,应在3个不同的轨道,符合洪特规则、泡利不相容原理;
②2p能层有4个电子,同一个原子轨道中不应有自旋状态相同的电子,违反了泡利原理;
③3d能级中有5个不同的轨道,对于基态原子,电子在能量相同的轨道上排布时,将尽可能分占不同的轨道并且自旋状态相同,违反了洪特规则;
④3d能级中有5个不同的轨道,有10个电子,符合洪特规则、泡利不相容原理;
⑤3d能级中有5个不同的轨道,有6个电子,图示不同轨道的单电子自旋方向不同,违反了洪特规则;
故答案为:②;③⑤.
点评 本题考查原子核外电子的排布,题目难度不大,注意泡利原理、洪特规则的内容即可解答该题,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
15.两种短周期元素A和B可组成的化合物中,A和B原子个数比为1:2,已知A的原子序数为m时,B的原子序数为:①m+2 ②m+3 ③m+4 ④m+5 ⑤m+8 ⑥m-7 ⑦m-8中的几种.其中不符合题目要求的是( )
| A. | ①④ | B. | ②⑥ | C. | ③⑤ | D. | ⑥⑦ |
16.已知:H2(g)+F2(g)═2HF(g)△H=-270kJ•mol-1,下列说法不正确的是( )
| A. | 44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收270 kJ热量 | |
| B. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于270 kJ | |
| C. | 相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量 | |
| D. | 2 mol H-F键的键能比1 mol H-H键和1 mol F-F键的键能之和大270 kJ |
13.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 为防止中秋月饼等富脂等食品被氧化,常在包装中放入还原铁粉等 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率,属于牺牲阴极的阳极保护法 | |
| C. | 镀层破坏后,镀锡铁板比镀锌铁板更易腐蚀 | |
| D. | 电解熔融MgCl2,可制得金属镁 |
20.实验室中能用磨口玻璃瓶保存的是( )
| A. | NaOH | B. | 盐酸 | C. | 水玻璃 | D. | 氢氟酸 |
10.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全: NH4++H++SO42-+Ba2++2OH-=NH3•H2O+BaSO4↓+H2O | |
| B. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O | |
| C. | 用铜作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 以下有机物在碱性条件下水解的化学方程式: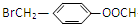 +3NaOH$\stackrel{△}{→}$ +3NaOH$\stackrel{△}{→}$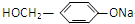 +HCOONa+NaBr +HCOONa+NaBr |
17.下列化学反应的离子方程式正确的是( )
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 用CH3 COOH溶解CaC03:CaCO3+2H+═Ca++H2O+CO2↑ | |
| C. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO${\;}_{4}^{2-}$+2Ba2++4OH-═2BaSO4↓+AlO${\;}_{2}^{-}$+2H2O | |
| D. | 用硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO${\;}_{4}^{-}$+6H++5H2O2═2Mn2++5O2↑+8H2O |
14.下列关于金属单质及其化合物的叙述正确的是
①赤铁矿的主要成分是Fe3O4
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
⑤Fe3+与KSCN产生血红色沉淀
⑥Na2O2既可作呼吸面具中,又可漂白织物、麦杆、羽毛等
⑦铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
⑧明矾常作为消毒剂
⑨氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得到相同的物质( )
①赤铁矿的主要成分是Fe3O4
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
⑤Fe3+与KSCN产生血红色沉淀
⑥Na2O2既可作呼吸面具中,又可漂白织物、麦杆、羽毛等
⑦铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物
⑧明矾常作为消毒剂
⑨氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得到相同的物质( )
| A. | ④⑥⑧ | B. | ①③④⑥⑦ | C. | ②④⑥⑦⑨ | D. | ①②③⑤⑧ |
15.在酸性溶液中,下列各组离子能大量共存的是( )
| A. | NH${\;}_{4}^{+}$、K+、Al3+、SO${\;}_{4}^{2-}$ | B. | Cl-、I-、K+、MnO${\;}_{4}^{-}$ | ||
| C. | Na+、S2O${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$、K+ | D. | Na+、NO${\;}_{3}^{-}$、PO${\;}_{4}^{3-}$、Cl- |