题目内容
已知热化学方程式C2H2(g)+5/2O2(g)=2CO2(g)+H2O(g);△H=-1256kJ/mol,下列说法正确的是
| A.乙炔的燃烧热为1256kJ/mol |
| B.若转移10mol电子,则消耗2.5mol O2 |
| C.若生成2mol液态水,则△H=-2512kJ/mol |
| D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ |
B
燃烧热是在一定条件下,1mol可燃物完全燃烧,生成稳定的氧化物时放出的热量,水的稳定状态时液态,A、C不正确;氧气得到4个电子,10mol电子,相应2.5mol氧气,B正确;形成4mol碳氧共用电子对,生成1molCO2,所以放出的热量是628kJ,D不正确,答案选B。

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
 2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
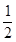 H2(g)+
H2(g)+