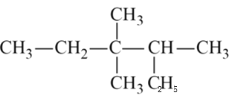
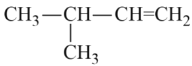题目内容
【题目】从海水中提取镁的工艺流程可表示如下:

下列说法不正确的是( )
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl2时阴极产生氯气
C.上述工艺流程中涉及化合、分解和复分解反应步骤
D.⑤可将晶体置于HCl气体氛围中脱水
【答案】B
【解析】
由海水中提取镁的工艺流程可知,贝壳高温煅烧,贝壳中的碳酸钙分解生成氧化钙,氧化钙与水反应制得石灰乳;向海水结晶、过滤后的母液中加入石灰乳,母液中镁离子与石灰乳反应生成氢氧化镁沉淀,向过滤得到的氢氧化镁沉淀中加入盐酸,氢氧化镁沉淀溶于盐酸制得氯化镁溶液,氯化镁溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到六水合氯化镁晶体,六水合氯化镁晶体在氯化氢气流中加热脱水得到无水氯化镁,电解熔融氯化镁制备镁。
A项、海水中镁元素含量高,原料来源于海水,提取镁原料来源丰富,故A正确;
B项、电解熔融MgCl2时,镁离子在阴极得电子发生还原反应生成镁,氯离子在阳极失电子发生氧化反应生成氯气,故B错误;
C项、上述工艺流程中贝壳分解涉及分解反应,得到石灰乳涉及化合反应,③④为复分解反应,最后两个反应都是分解反应,故C正确;
D项、若直接加热MgCl26H2O,氯化氢挥发会促进MgCl2水解,使水解趋于完全得不到无水MgCl2,因Mg2+水解呈酸性,在氯化氢气流中可抑制Mg2+水解,同时带走水蒸气,故一定条件为在HCl气流中,目的是抑制Mg2+水解,故D正确;
答案选B。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】PbCO3可用于油漆、陶瓷和玻璃等工业。由方铅矿(主要成分为PbS,含有杂质FeS等)和软锰矿(主要成分为MnO2)制备PbCO3的流程如下:
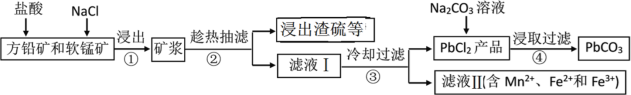
已知:PbCl2难溶于冷水和乙醇,易溶于热水;各物质的溶度积见表。试回答下列问题:
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | PbCl2 | PbS | PbCO3 |
Ksp | 2×10-13 | 8.0×10-16 | 1×10-38 | 1.6×10-5 | 8.0×10-28 | 7.4×10-14 |
(1)PbCO3的名称是________。
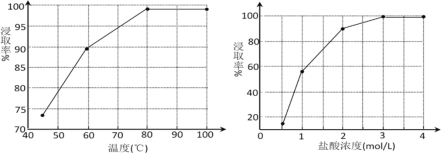
(2)步骤①中MnO2的作用是________,根据下图分析过程①的最佳反应条件是_________。
(3)步骤②趁热抽滤的原因是___________________。
(4)步骤③洗涤用的试剂是____________。
(5)将滤液Ⅱ先酸化,然后加入MnO2,反应的离子方程式为________;若反应后![]() ,进一步调节溶液的pH可分离出Fe3+和Mn2+,则调节溶液pH的范围为_________
,进一步调节溶液的pH可分离出Fe3+和Mn2+,则调节溶液pH的范围为_________![]() 时表示Fe3+已沉淀完全]。
时表示Fe3+已沉淀完全]。
(6)步骤④反应的离子方程式为______________。