题目内容
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.6.0gSiO2晶体中含有共价键的数目为 0.2NA
B.标准状况下,22.4L甲醇中含有的 C-H 键数目为 0.3NA
C.室温下,53.5gNH4Cl晶体溶于氨水中,所得溶液 pH=7,NH![]() 的数目为NA
的数目为NA
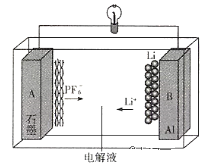
D.用铅蓄电池电解氯化钠溶液,得到22.4L H2,铅蓄电池中消耗氢离子数为4NA
【答案】C
【解析】
A. 1mol SiO2中含4molSi-O共价键,6.0gSiO2晶体的物质的量为0.1mol,含有共价键的数目为 0.4NA,A错误;
B. 标准状况下,甲醇不是气体,无法计算,B错误;
C. 53.5gNH4Cl晶体的物质的量为1mol,根据电荷守恒,c(NH4+)+c(H+)=c(Cl-)+c(OH-),pH=7可知,c(H+)=c(OH-),则c(NH4+)=c(Cl-)=1mol,NH![]() 的数目为NA,C正确;
的数目为NA,C正确;
D. 用铅蓄电池电解氯化钠溶液,标准状况下,得到22.4LH2,转移电子的物质的量为2mol,铅蓄电池的正极电极反应式为PbO2+2e+4H+=Pb2++2H2O,可知消耗4mol的氢离子,所以理论上铅蓄电池中耗氢离子个数为4NA,但生成的氢气不一定在标况下,D错误;故答案为:C。

练习册系列答案
相关题目